

 ,C
,C .
.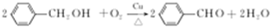 .
. .
. 含苯环的所有同分异构体的结构简式:
含苯环的所有同分异构体的结构简式: .
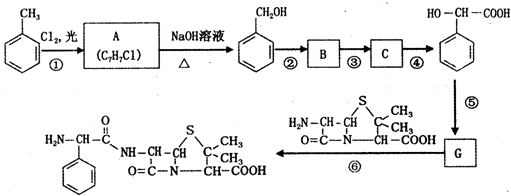
. 分析 甲苯与氯气发生一元取代生成A,A在氢氧化钠水溶液、加热条件下发生水解反应生成苯甲醇,则A为 .由反应④产物结构(
.由反应④产物结构( ),结合反应信息可知苯甲醇产生催化氧化生成B为
),结合反应信息可知苯甲醇产生催化氧化生成B为 ,苯甲醛与HCN发生加成反应C为
,苯甲醛与HCN发生加成反应C为 ,再酸化水解得到
,再酸化水解得到 ,对比反应⑥产物结构可知,G的结构简式为:
,对比反应⑥产物结构可知,G的结构简式为: ,据此解答.
,据此解答.
解答 解:甲苯与氯气发生一元取代生成A,A在氢氧化钠水溶液、加热条件下发生水解反应生成苯甲醇,则A为 .由反应④产物结构(
.由反应④产物结构( ),结合反应信息可知苯甲醇产生催化氧化生成B为
),结合反应信息可知苯甲醇产生催化氧化生成B为 ,苯甲醛与HCN发生加成反应生成C为
,苯甲醛与HCN发生加成反应生成C为 ,再酸化水解得到
,再酸化水解得到 ,对比反应⑥产物结构可知,G的结构简式为:
,对比反应⑥产物结构可知,G的结构简式为: .
.
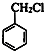
(1)由上述分析可知,A的结构简式为 ,C的结构简式为:
,C的结构简式为: ,
,
故答案为: ;
; ;
;
(2)反应①属于取代反应,反应③属于加成反应,
故答案为:取代反应;加成反应;
(3)G为 ,含有的官能团的名称为:羧基、氨基;反应④的反应条件为:H2O/H+,
,含有的官能团的名称为:羧基、氨基;反应④的反应条件为:H2O/H+,
故答案为:羧基、氨基;H2O/H+;
(4)②反应的化学方程式: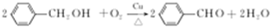 ,
,
故答案为: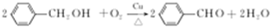 ;
;
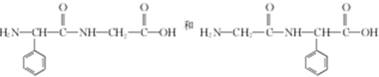
(5)甘氨酸(H2NCH2COOH)和G发生缩合生成二肽的结构简式: ,
,
故答案为: ;
;
(6) 含苯环的所有同分异构体的结构简式有:
含苯环的所有同分异构体的结构简式有: ,
,
故答案为: .
.
点评 本题考查有机物推断、有机反应类型、官能团结构与性质、同分异构体书写等,注意根据有机物的结构与反应信息进行推断,是对有机物化学的综合考查,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 55kJ | B. | 220kJ | C. | 550kJ | D. | 1108kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量;O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量;O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA | |
| D. | 常温常压下,22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  |  |  |
| ① | ② | ③ | ④ |
| A. | 装置①可用于模拟氯碱工业生产氯气 | |
| B. | 装置②的原理可用于潮汐能发电站钢阀门的保护 | |
| C. | 装置③可用于食盐水的蒸发结晶 | |
| D. | 装置④可用于二氧化锰与浓盐酸反应制取氯气 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 物质结构决定物质性质.回答下列问题:
物质结构决定物质性质.回答下列问题: ,其中心原子N的杂化方式是sp3.
,其中心原子N的杂化方式是sp3.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;Z基态原子的M层与K层电子数相等;R2+的3d轨道有9个电子.
X、Y、Z、R为前四周期元素,且原子序数依次增大.XY2是红棕色气体;Z基态原子的M层与K层电子数相等;R2+的3d轨道有9个电子.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一束光线分别通过溶液和胶体时,后者能看到一条光亮的“通路”,前者则没有 | |
| B. | 蔗糖、硫酸钡和氨气分别属于非电解质、强电解质和弱电解质 | |
| C. | Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到 | |
| D. | 沼气、天然气和水煤气分别属于化石能源、可再生能源和二次能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com