
| A.HNO3 | B.Br2 | C.ClO- | D.MnO4- |
科目:高中化学 来源:不详 题型:单选题
| A.人类使用的物质都是纯度越高越好 |
| B.分子是保持物质化学性质的一种微粒,如果分子的组成或结构变了其化学性质就变了 |
| C.定量研究的方法是化学发展为一门科学的重要标志 |
| D.改变物质的性质不一定要通过化学变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
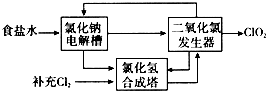
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1mol | B.0.05mol | C.1.05mol | D.0.11mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.15mol | B.0.2mol | C.0.3mol | D.0.4mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| x-8 |
| ||
| 加热 |
| 2-4 |
| -4 |
| x-8 |
| A.0 | B.1 | C.2 | D.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.铁粉中混有锌粉杂质(稀硫酸) |
| B.FeCl3中混有FeCl2杂质(Cl2) |
| C.CO气体中混有CO2杂质(NaOH溶液) |
| D.SiO2中混有CaCO3杂质(盐酸) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com