
A.燃烧热的集中表现 B.中和热的集中表现
C.溶解热的集中表现 D.键能变化的集中表现
科目:高中化学 来源: 题型:阅读理解
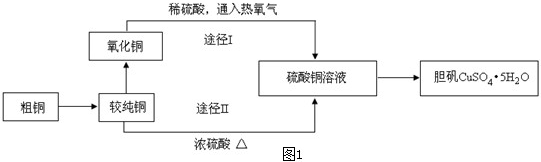
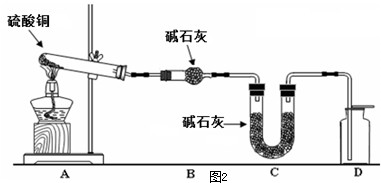
| 装置 | A(试管+粉末) | B | C |
| 反应前 | 50.0g | 70.0g | 540.0g |
| 反应后 | 45.0g | 74.5g | 540.0g |
查看答案和解析>>
科目:高中化学 来源:江苏省梅村高级中学2012届高三12月双周练化学试题 题型:022
某混合动力车,可以用电动机、内燃机或二者结合推动车轮.汽车上坡或加速时,电动机提供推动力,降低了汽油的消耗;在刹车和下坡时电动机处于充电状态.
(1)混合动力车的内燃机以汽油为燃料,汽油(以辛烷C8H18计)和氧气充分反应,每生成1 mol水蒸气放热569.1 kJ.则该反应的热化学方程式为________.
(2)混合动力车的电动机目前一般使用的是镍氢电池,镍氢电池采用镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解液.镍氢电池充放电原理示意如图,其总反应式是:
 H2+2NiOOH
H2+2NiOOH根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH将________(填“增大”、“不变”或“减小”),该电极的电极反应式为________.
(3)汽车尾气中的一氧化碳是大气污染物,可通过如下反应降低其浓度:CO(g)+1/2O2(g)![]() CO2(g).
CO2(g).
①某温度下,在两个容器中进行上述反应,容器中各物质的起始浓度及正逆反应速率关系如下表所示.请填写表中的空格.

②相同温度下,某汽车尾气中CO、CO2的浓度分别为1.0×10-5 mol·L-1和1.0×10-4mol·L-1.若在汽车的排气管上增加一个补燃器,不断补充O2并使其浓度保持为1.0×10-4 mol·L-1,则最终尾气中CO的浓度为________mol·L-1.
(4)汽车尾气中的NOx是另一种大气污染物,可用NH3在催化剂存在下净化,写出该反应的化学方程式________.当参加反应的NH3在标准状况下体积为a L时,还原产物的质量为________g
查看答案和解析>>
科目:高中化学 来源:2013-2014学年上海市普陀区高三上学期质量调研化学试卷(解析版) 题型:实验题
硫酸铜晶体俗称“胆矾”,在无机化工及生产生活中有广泛的应用。某课外研究小组的同学用粗铜粉(含有碳等杂质)设计了两种制备胆矾的途径,并测定了其中结晶水的含量。设计的流程如下:

(1)“较纯铜”转化为氧化铜时,应将其置于 内进行灼烧(填写仪器名称)。“粗铜”表面的油脂可以用热碱溶液洗去,原因是 。若灼烧“粗铜”,获得的产物是混有少量铜的氧化铜。存在少量铜的可能原因是 。
a.灼烧过程中部分氧化铜被还原 b.该条件下铜无法被氧气氧化
c.氧化铜在加热过程中分解生成铜 d.灼烧不充分铜未被完全氧化
(2)通过途径I实现用粗制氧化铜制取胆矾,必须进行的实验操作步骤是:酸溶、加热通氧气、过滤、 、冷却结晶、 、自然干燥。比较由粗制氧化铜制取胆矾的两种途径,途径Ⅰ有明显的两个优点:
① 。
② 。
(3)测定胆矾晶体里结晶水的含量时,若测定的相对误差大于零,则产生误差的原因可能是___________。
a.加热后容器未放入干燥器中冷却
b.最后两次加热后的质量相差较大
c.加热前称量时容器未完全干燥
d.加热过程中有少量溅失
(4)利用下图装置加热无水硫酸铜粉末直至完全分解,A的试管中剩余黑色粉末,用带火星的木条伸入集气瓶D,发现木条能复燃。反应前后各装置的质量见图下方的表格所示。
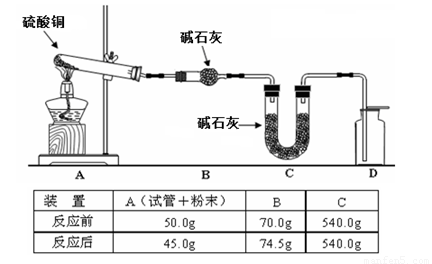
请通过计算,推断该实验条件下硫酸铜分解的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源:2014届广东省高一上学期期末考试化学试卷 题型:选择题
下列叙述中正确的是
A.二氧化碳能灭火,所以燃着的镁条在二氧化碳中便熄灭。
B.硬铝的硬度比铝大,熔点比铝低。
C.相同质量的铜分别跟足量的浓硝酸或稀硝酸反应,产生气体的体积比为1∶1。
D.相同质量的铝分别跟足量的稀盐酸酸或氢氧化钠溶液共热,产生气体体积相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列关于实验的叙述正确的是 。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.在两支试管里分别加热NH4Cl和NH4HCO3,现象完全相同
C.在铝热反应的实验中,用滤纸做的漏斗必须干燥
D.用滴有酚酞的水做氨的喷泉实验,只验证了氨的溶解性
E.验证CO2中混有SO2时,可将混俣气体通过品红溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com