
【题目】下列有关说法不正确是( )
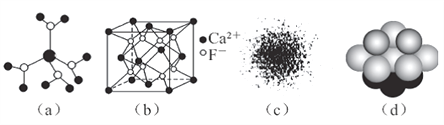
A. 水合铜离子的模型如图(a)所示,1个水合铜离子中有4个配位体
B. CaF2晶体的晶胞如图(b)所示,每个CaF2晶胞平均占有4个Ca2+
C. H原子的电子云图如图(c)所示,H原子核外大多数电子在原子核附近运动
D. 金属Cu中Cu原子堆积模型如图(d),为最密堆积,每个Cu原子的配位数均为12
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源: 题型:
【题目】常见的分类法有交叉分类法、树状分类法等。无机化合物可根据其组成和性质进行分类:
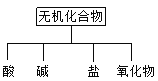
(1)上图所示的物质分类方法名称是_______________________。
(2)以Na、H、O、N、C中两种或三种元素组成合适的物质,分别填在下表①④⑦处。
物质类别 | 酸 | 碱 | 盐 | 氧化物 |
化学式 | ① _________②HNO3 | ③NH3H2O ④________ | ⑤Na2CO3 ⑥NaNO3 ⑦_______ | ⑧CO2 ⑨Na2O2 |
(3)在②③⑤⑥⑧⑨六种物质中,属于非电解质的是______________(填序号)。
(4)过量⑧通入④中发生反应的离子方程式为:______________________________________________。⑧与⑨反应的化学方程式为:______________________________。
(5)15.9g⑤溶于水配制成250mL溶液,CO32-的粒子数为__________,Na+的物质的量浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把18.0mol/L的浓硫酸稀释成1.2mol/L的稀硫酸250mL。
(1)1.2mol/L的稀硫酸的含义是__________(选填字母)。
A.1L水中含有1.2mol H2SO4
B.1L溶液中含有1.2mol H+
C.将117.6g硫酸溶于1L水所配成的溶液
D.从100mL该溶液中取出10mL,剩余溶液的物质的量浓度仍为1.2mol/L
(2)请在下列操作步骤中填写有关的空格:
①用量筒量取_________mL的18.0mol/L的浓硫酸;
②将_______________沿烧杯内壁慢慢注入盛有少量____________的烧杯中;
③将已冷却至室温的硫酸溶液沿玻璃棒注入_________mL的容量瓶中;
④用少量蒸馏水洗涤烧杯2~3次,并将洗涤液也全部转移到容量瓶中;
⑤继续向容量瓶中加蒸馏水,直至液面接近刻度线1~2cm处;
⑥改用___________________逐滴加蒸馏水,使溶液凹液面恰好与刻度线相切;
⑦盖好容量瓶塞,反复颠倒,摇匀;
⑧将配好的稀硫酸倒入试剂瓶中,贴好标签。
(3)由于操作不当,会引起实验误差。下列情况对所配制的H2SO4溶液的物质的量浓度有何影响?(用“偏高”、“偏低”、“无影响”填空)。
①容量瓶用蒸馏水洗涤后残留有少量的水_____________;
②定容时,某同学观察液面的情况如图所示_____________;

③摇匀后,发现溶液的液面低于刻度线,又加水至刻度线____________。
(4)某同学取配制的1.2mol/L的稀硫酸100mL,向其中加入足量的锌粒,产生的H2在标准状况下的体积为_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,下列各组离子能大量共存的是( )
A. 稀硫酸中:K+、Mg2+、A1O2-、S2O32-
B. KW/c(H+)=10-13 mol·L-1 的溶液中:Fe3+、NH4+、Mg2+、SO42-
C. 使甲基橙变红的溶液中:Fe2+、MnO4﹣、Na+、SO42﹣
D. 通入大量 CO2 的溶液中:Na+、ClO-、CH3COO-、HCO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值。下列叙述不正确的是( )
A. 足量锌与一定量浓H2SO4反应生成0.5mol气体,反应中转移的电子数为NA
B. 1L 0.1mol/L的CH3COOH溶液中含有H+的数目约为0.1 NA
C. 电解精炼铜(粗铜中含有锌、铁、银等杂质),电路中有2NA个电子通过时,阴极增重64g
D. 常温常压下,1.8 g甲基(-CD3)中含有的电子数为0.9NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】张亭栋研究小组受民间中医启发,发现As2O3(俗称砒霜)对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)等都是VA族的元素,该族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)NH3的沸点比PH3_____(填“高"或“低”),原因是_____________。
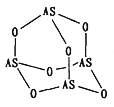
(2)Na3AsO4 中含有的化学键类型包括_______;AsO43-的空间构型为_______,As4O6的分子结构如图所示,则在该化合物中As的杂化方式是_________。
(3)自然固氮现象发生的一系列化学变化:N2→NO→NO2→HNO3→NO3-解释了民谚“雷雨发庄稼”的原理。
①NO3-中N原子采取_____杂化方式,其空间构型为________,写出它的一种等电子体的化学式________.
②已知酸性: HNO3>HNO2,下列相关见解合理的是_________.
A.含氧酸中氧原子总数越多,酸性越强
B.同种元素化合价越高,对应含氧酸的酸性越强
C.HNO3中氮元素的正电性更高,在水溶液中更易电离出H+,酸性强于HNO2
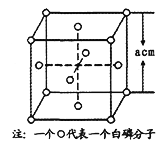
(4)白磷(P4)的晶体属于分子晶体,其晶胞结构如图(小圆圈表示白磷分子)。己知晶胞的边长为acm,阿伏加德罗常数为NA mol-1,则该晶胞中含有的P原子的个数为______,该晶体的密度为______g·cm-3(用含NA、a的式子表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲烷与Cl2的取代反应所得四种有机产物的说法不正确的是( )
A.都是有机物B.都不溶于水
C.有一种气态物质,其余均是液体D.均是正四面体结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香豆素是一种用途广泛的香料,可用于配制香精以及制造日用化妆品和香皂等。以有机物M和有机物A合成香豆素的流程如下:

已知以下信息:
①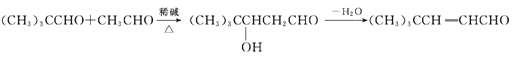
② M的分子式为C2H6O,分子中有3种化学环境不同的氢原子
③ 香豆素中含有两个六元环
(l) M的化学名称是______,由M生成B的化学方程式为_______。
(2) A的结构简式为________。
(3) D转变为E的第①步所需的试剂及反应条件是________。
(4)由E生成香豆素的化学方程式为________。
(5)写出满足如下条件的C的一种同分异构体的结构简式:________。
① 能发生银镜反应 ② 1mol C完全反应能消耗2 mol NaOH
③ 苯环上有3个取代基 ④ 苯环上的一氯代物只有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com