
下列关于化学与生产、生活的认识不正确的是
A.普通铅笔芯的主要成分是铅
B.煤的气化和液化过程均属化学变化
C.硅酸钠溶液俗名水玻璃,可用于制备硅胶和木材防火剂
D.合理开发利用可燃冰(固态甲烷水合物)有助于缓解能源紧缺
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
Li—Al/FeS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:
2Li++FeS+2e-====Li2S+Fe。有关该电池的下列叙述中正确的是 ( )
A.Li—Al在电池中作为负极材料,该材料中Li的化合价为+1价
B.该电池的电池反应式为2 Li+FeS =Li2S+Fe
C.负极的电极反应式为Al-3e-===Al3+
D.充电时,阴极发生的电极反应式为Li2S+Fe-2e-===2Li++FeS
查看答案和解析>>
科目:高中化学 来源: 题型:
有机合成粘合剂是生产和生活中一类重要的材料,粘合的过程一般是呈液态的粘合剂小分子,经化学反应转化为大分子或高分子而固化。“502胶”是一种快干胶,其为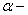 氰基丙烯酸乙酯:
氰基丙烯酸乙酯:
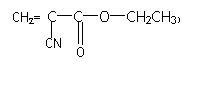 |
当暴露在空气中时,微量的水起催化作用,使其发生碳碳键的加聚反应而迅速固化,几秒钟即可把粘物牢牢粘在一起,请写出“502胶”发生粘合作用的化学方程式:
_______________________________________,反应类型:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
MOH和ROH两种一元碱的溶液分别加水稀释时,
pH变化。如右图所示。下列叙述中正确的是
A.ROH是一种弱碱
B.在x点,c(M+) = c(R+)
C.在x点, MOH完全电离
D.稀释前,c(ROH) =10 c(MOH)
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大的伤害,必须进行处理。某工厂使用还原沉淀法处理,该法的工艺流程为:
 |
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若平衡体系的pH=12,则溶液显 色。
(2)能说明第①步反应达平衡状态的是 。
a.Cr2O72-的浓度不变 b.Cr2O72-和CrO42-的浓度相同
c.2v(Cr2O72-)=v(CrO42-) d.溶液的颜色不变
(3)第②步反应中,还原剂为 ,该还原剂反应后生成 。
(4)电镀废液中Cr2O72-还可通过下列反应转化:
Cr2O72-(aq)+2Pb2+(aq)+H2O(l) 2 PbCrO4(s)+2H+(aq) ΔH< 0
2 PbCrO4(s)+2H+(aq) ΔH< 0
该反应达平衡后,改变横坐标表示的反应条件,下列示意图正确的是
[]
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是
A.H2S的稳定性比HF的稳定性强
B.某元素X的气态氢化物的化学式为H2X,则其最高价氧化物的化学式为XO3
C.离子化合物中可能含有共价键,共价化合物中可能含有离子键
D.一个D2O分子所含的中子数为8
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,下列各溶液中,离子的物质的量浓度关系正确的是
A.pH=3的盐酸中:c(H+)=3.0mol·L-1
B.0.1mol·L−1的碳酸钠溶液中:c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol·L-1
C.氯化铵溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.碳酸氢钠溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
将20mLNO2和NH3的混合气体,在一定条件下充分反应, 化学方程式是:6NO2+8NH3
化学方程式是:6NO2+8NH3 7N2+12H2O。已知参加反应的NO2比NH3少2mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH
7N2+12H2O。已知参加反应的NO2比NH3少2mL(气体体积均在相同状况下测定),则原混合气体中NO2和NH 3的物质的量之比是( )
3的物质的量之比是( )
A.3∶2 B.2∶3 C.3∶7 D.3∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com