
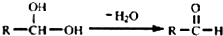

 ��
�� ��
�� ��
�� ��ֻд��һ�ּ��ɣ�
��ֻд��һ�ּ��ɣ� ���� A����ˮ�ⷴӦC��D��E��C������D������������Ϣ��֪��C�Ľṹ��ʽΪCH3CHO��DΪCH3COONa��EΪNaBr��B������ʺɱ�Ϊ208������B����Է�������Ϊ208�����������ʾB�����к��б����ṹ�������������˴Ź�����������������շ壬���ֵ��Ϊ2��2��2��3��3�����б����ϵ�һ�ȴ���ֻ�����֣�B����ˮ���D��C����BΪ ��B����ˮ���FΪ
��B����ˮ���FΪ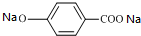 ��GΪCH3CH2OH����CH3CH2OHΪԭ�Ϻϳ���������������CH3COCH2COOC2H5�������������Ҵ����������ᣬ�Ҵ����Ҵ����������������������������Ƶ������·���������Ϣ�еķ�Ӧ�����������������ݴ˷������
��GΪCH3CH2OH����CH3CH2OHΪԭ�Ϻϳ���������������CH3COCH2COOC2H5�������������Ҵ����������ᣬ�Ҵ����Ҵ����������������������������Ƶ������·���������Ϣ�еķ�Ӧ�����������������ݴ˷������
��� �⣺A����ˮ�ⷴӦC��D��E��C������D������������Ϣ��֪��C�Ľṹ��ʽΪCH3CHO��DΪCH3COONa��EΪNaBr��B������ʺɱ�Ϊ208������B����Է�������Ϊ208�����������ʾB�����к��б����ṹ�������������˴Ź�����������������շ壬���ֵ��Ϊ2��2��2��3��3�����б����ϵ�һ�ȴ���ֻ�����֣�B����ˮ���D��C����BΪ ��B����ˮ���FΪ
��B����ˮ���FΪ ��GΪCH3CH2OH����CH3CH2OHΪԭ�Ϻϳ���������������CH3COCH2COOC2H5�������������Ҵ����������ᣬ�Ҵ����Ҵ����������������������������Ƶ������·���������Ϣ�еķ�Ӧ����������������
��GΪCH3CH2OH����CH3CH2OHΪԭ�Ϻϳ���������������CH3COCH2COOC2H5�������������Ҵ����������ᣬ�Ҵ����Ҵ����������������������������Ƶ������·���������Ϣ�еķ�Ӧ����������������
��1��A�����������ŵ�����Ϊ��������ԭ�ӣ��ʴ�Ϊ����������ԭ�ӣ�
��2��ͨ�����Ϸ���֪��B�Ľṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��3����ͼ��ת����ϵ�У�����������ʱ��Ӧ�����Ǽӳɷ�Ӧ����ѡB��
��4����Ӧ�ٵķ���ʽΪ ����Ӧ �ܵķ���ʽΪ
����Ӧ �ܵķ���ʽΪ ��
��
�ʴ�Ϊ�� ��
�� ��
��
��5��FΪ ����F�м���ϡH2SO4��ͻ�������һ���л���HΪ���ǻ������ᣬH��ͬ���칹���������������
����F�м���ϡH2SO4��ͻ�������һ���л���HΪ���ǻ������ᣬH��ͬ���칹���������������
����FeCl3��ɫ��˵�����з��ǻ���
���ܷ���������Ӧ��˵������ȩ����
�������-OH��HCOO-���ڼ�����ֽṹ��
�����������-OH��-CHO��
�������������λ����2��ͬ���칹�壻
�������-OH���ڼ�λ����3��ͬ���칹�壻
�������-OH���ڶ�λ����1��ͬ���칹�壬���Է�����������9�֣�
�ʴ�Ϊ��9��
��6����5���б�����һ�ȴ���ֻ�����ֵ�ͬ���칹��ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ�����������ȷ��B�ķ���ʽ�ǽⱾ��ؼ��������л���Ĺ����ŵı仯Ϊͻ�ƿڽ����ƶϣ���Ҫѧ���������չ����ŵĽṹ�����ʣ��ѵ���ͬ���칹�������жϣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
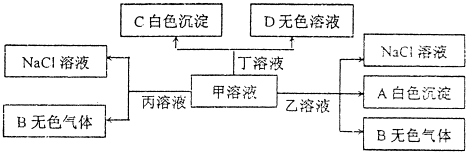
| A�� | ��ΪAlC13 | |
| B�� | �ܴ�����������Һ���е����ӣ�Fe3+��SO42-��NO3- | |
| C�� | ����Һ�����ӵĵ�����ϵ��c��Na+��=c��HCO3-��+c��CO32-��+c��H2CO3�� | |
| D�� | ����Һ�еμ���������Һ��Ӧ�����ӷ���ʽ��HCO3-+Ba2++OH-�TBaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
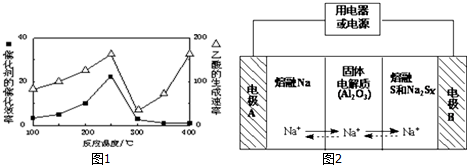
| ���� | Na | S | Al2O3 |
| �۵�/�� | 97.8 | 115 | 2050 |
| �е�/�� | 892 | 444.6 | 2980 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | lmol H2O2�����еķǼ��Թ��ۼ���ΪNA | |
| B�� | 1L 0��lmol•L-1��NaHCO3��Һ��HCO3-��CO32-������֮��Ϊ0.1NA | |
| C�� | �����������ⸯʴʱ��0.56gFe��Ӧת�Ƶ�����Ϊ0.03NA | |
| D�� | ����ȼ�ϵ����������22.4L����ʱ����·��ͨ���ĵ�����ĿΪ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺
���ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã���ش��������⣺| t/K | 298 | 398 | 498 | �� |
| K/��mol•L-1��-2 | 4.1��106 | K1 | K2 | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ��Һ�У�H+��I-��NO3-��SiO32- | |
| B�� | ������ˮ�У�Cl-��NO3-��Na+��SO32- | |
| C�� | ������Һ�У�NO3-��I-��Na+��Fe2+ | |
| D�� | ������CO2ͨ��ʱ��H+��NH4+��Al3+��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ������������ѧ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
A����֪�����Ȼ�ѧ����ʽ��
��CH3COOH(l)��2O2(g)=2CO2(g)��2H2O(l) ��H1����870.3 kJ/mol
��C(s)��O2(g)= CO2(g) ��H2����393.5 kJ/mol
��H2(g)��1/2O2(g)=H2O(l) ��H3����285.8 kJ/mol
��Ӧ��2C(s)��2H2(g)��O2(g)=CH3COOH(l)���ʱ�Ϊ
b .��H2(g)��1/2O2(g)=H2O(l) ��H����285��8 kJ/mol
.��H2(g)��1/2O2(g)=H2O(l) ��H����285��8 kJ/mol
��H2(g)��1/2O2(g)=H2O(g) ��H����241��8 kJ/mol
��C(s)��1/2O2(g)=CO(g) ��H����110��5 kJ/mol
��C(s)��O2(g)=CO2(g) ��H����393��5 kJ/mol
�ش��������⣺
��1��������Ӧ�����ڷ��ȷ�Ӧ���� ��
��2��H2��ȼ����Ϊ ��C��ȼ����Ϊ ��
��3��CO��ȼ����Ϊ �����Ȼ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com