
【题目】将0.46mol SO2和0.22mol氧气放入容积为2L的密闭容器中,发生反应2SO2 (g)+O2 (g)2SO3 (g),在一定温度下,反应达到平衡,得到0.24mol SO3 , 则反应的平衡常数K= . 若温度不变,再加入1.0mol氧气后重新达到平衡,则SO2的平衡浓度(填“增大”、“不变”或“减小”),氧气的转化率(填“升高”、“不变”或“降低”),SO3的体积分数(填“增大”、“不变”或“减小”).
【答案】23.8;减小;降低;减小
【解析】解:将0.46mol SO2和0.22mol氧气放入容积为2L的密闭容器中,发生反应2SO2 (g)+O2 (g)2SO3 (g),在一定温度下,反应达到平衡,得到0.24mol SO3 , 则:
2SO2(g)+ | O2(g) | 2SO3(g) | ||
起始浓度(mol): | 0.23 | 0.11 | 0 | |
变化浓度(mol): | 0.12 | 0.06 | 0.12 | |
平衡浓度(mol): | 0.11 | 0.05 | 0.12 |
则化学平衡常数K= ![]() =
= ![]() =23.8;
=23.8;
若温度不变,再加入1.0mol氧气,则平衡正向移动,重新达到平衡,则 SO2的平衡浓度增大,但氧气的转化率降低,
2SO2(g)+ | O2(g) | 2SO3(g) | ||
起始浓度(mol): | 0.22 | 0.1+1.0 | 0.24 | |
变化浓度(mol): | 2x | x | 2x | |
二次平衡(mol): | 0.22﹣2x | 1.1﹣x | 0.24+2x |
二次平衡时SO3的体积分数: ![]() =
= ![]() ,而x的极大值为0.1,故
,而x的极大值为0.1,故 ![]() 的极大值为30%,三氧化硫的体积分数减小;
的极大值为30%,三氧化硫的体积分数减小;
所以答案是:23.8; 减小; 降低;减小.
【考点精析】掌握化学平衡状态本质及特征和化学平衡的计算是解答本题的根本,需要知道化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
【题目】有三种不同质量比的氧化铜与炭粉的混合物样品①、②、③.甲、乙、丙三同学各取一种样品,加强热充分反应,测定各样品中氧化铜的量.
(1)甲取样品①强热,若所得固体为金属铜,将其置于足量的稀硝酸中微热,产生1.12L气体(标准状况),则样品①中氧化铜的质量为g.
(2)乙取样品②ag强热,生成的气体不能使澄清的石灰水变浑浊.再将反应后的固体与足量的稀硝酸微热,充分反应后,有bg固体剩余,该剩余固体的化学式为 . 样品②中氧化铜质量为g (以含a、b的代数式表示).
(3)丙称量样品③强热后剩余的固体,质量比原样品减小了cg,若该固体为金属铜,则样品③中氧化铜物质的量(n)的取值范围为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完全燃烧2mol某有机物,生成4molCO2和6molH2O,同时消耗5molO2,该有机物的分子式为
A. C2H6O2 B. C2H4O
C. C2H6O D. C2H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】进行过滤操作应选用的一组仪器是( )
A. 滤纸、烧杯、试管、漏斗、玻璃棒
B. 烧杯、酒精灯、试管、漏斗
C. 漏斗、玻璃棒、烧杯、铁架台、滤纸
D. 玻璃棒、滤纸、蒸馏烧瓶、漏斗、铁架台
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知草酸H2C2O4是二元弱酸.室温下向10mL 0.01molL﹣1 H2C2O4溶液中逐滴加入0.01molL﹣1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( ) 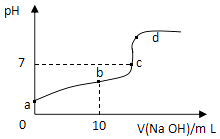
A.a点pH>2
B.b点表示的溶液中c(C2O42﹣)>c(H2C2O4)
C.c点时加入NaOH溶液的体积为20mL
D.d点存在c(Na+)+c(H+)=c(OH﹣)+2c(C2O42﹣)+c(HC2O4﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把18.0mol/L的浓硫酸稀释成1.8mol/L的稀硫酸100ml,实验操作如下:
A. 将配好的稀硫酸倒入试剂瓶中,贴好标签;
B. 盖好容量瓶塞,反复颠倒,摇匀;
C. 用量筒取…………mL的18.0mol/L的浓硫酸;
D. 将…………沿烧杯内壁慢慢注入盛有少量…………的烧杯中;
E. 用少量蒸馏水洗涤烧杯2﹣3次,并将洗涤液也全部转移到容量瓶中;
F. 将已冷却至室温的硫酸溶液沿玻璃棒注入100mL的容量瓶中;
G. 改用胶头滴管逐滴加蒸馏水,使溶液凹面恰好与刻度相切;
H. 继续向容量瓶加蒸馏水,直到液面接近刻度线…………cm处.
(1)填写上述步骤中的空白;
(2)请按正确的操作步骤进行排序 .
(3)试分析下列操作会使所配溶液的浓度会大于1.80mol/L浓度
A.用量筒取浓硫酸时,为了精确,用水洗涤量筒,并将洗涤液倒入烧杯中.
B.溶解后,立刻移液.
C.若加蒸馏水超过了刻度线,倒出一些溶液,再重新加蒸馏水到刻度线.
D.若定容时仰视看刻度线,会使稀硫酸溶液的浓度.
E.若摇匀后发现液面低于刻度线,又加水至刻度线.
(4)取20ml配好的硫酸,和足量的铝反应后,可收集到标准状况下的H2ml.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在相同条件下,下面各组热化学方程式中,△H1>△H 2的是( )
A.2H2(g)+O2(g)=2H2O(L);△H1????? 2H2(g)+O2(g)=2H2O(g);△H2
B.S(g)+O2(g)=SO2(g);△H1????? S(s)+O2(g)=SO2(g)△H2
C.H2(g)+Cl2(g)=2HCl(g);△H1 ![]() H2(g)+
H2(g)+ ![]() Cl2(g)=HCl(g);△H2
Cl2(g)=HCl(g);△H2
D.C(s)+ ![]() O2(g)=CO(g);△H1??????? C(s)+O2(g)=CO2(g);△H2
O2(g)=CO(g);△H1??????? C(s)+O2(g)=CO2(g);△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】蒸发操作中必须用到蒸发皿,下面对蒸发皿的操作中正确的是
A. 将蒸发皿放置在铁架台的铁圈上,并加垫石棉网加热
B. 将蒸发皿放置在铁架台的铁圈上直接用酒精灯火焰加热
C. 将灼热的蒸发皿直接放在冷水中冲洗
D. 将灼热的蒸发皿用手拿离火焰,直接放在实验台上
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com