
ij�л���A��ѧʽΪC3H6O3��1molA����2molNa��Ӧ��A�������������ţ���������������ͬһ��̼ԭ���ϡ�
��1��A�Ľṹ��ʽ�� _____________________��������������____________________
��2��A��ŨH2SO4���ȵ������¿���������Ԫ��״���ʣ�д���ⷴӦ�Ļ�ѧ����ʽ_____________________��Ӧ����Ϊ��_____________________
��3��A��ŨH2SO4���ȵ������·�����ȥ��Ӧ����B��B��һ�������¿��Ժϳ��л��߷���C��д��B����C�Ļ�ѧ����ʽ________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ��ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ڳ����·������з�Ӧ��
��16H����10Z����2XO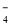 == 2X2����5Z2��8H2O
== 2X2����5Z2��8H2O
��2A2����B2 == 2A3����2B��
��2B����Z2 == B2��2Z�� ������������Ӧ���ж����н����д������( )
A����Һ�п��ܷ�����Ӧ��Z2��2A2��=2A3����2Z��
B��Z�ڢ٢۷�Ӧ������ԭ��
C��������ǿ��˳��ΪXO ��Z2��B2��A3��
��Z2��B2��A3��
D��X2����XO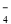 �Ļ�ԭ����
�Ļ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ�����ϵڶ��νβ⻯ѧ�Ծ��������棩 ���ͣ������
��ҵ�Ͽ������̿�(��Ҫ�ɷ���MnO2)�ͻ�����(��Ҫ�ɷ���FeS2)Ϊ��Ҫԭ���Ʊ������ܴ��Բ���̼����(MnCO3)���乤ҵ�������£�

��֪��MnCO3������ˮ���Ҵ�����ʪʱ�ױ�����������100�濪ʼ�ֽ⡣
�ش��������⣺
��1�����������Ŀ���dz�ȥ��Һ�е�Cu2+��Ca2+�����ʡ��������Һ��c(F-)=0.01mol/L-1����Һ�в�����c(Ca2+)= ����֪��Ksp(CaF2)=1.46��10-10��
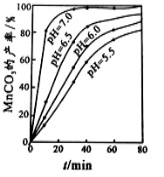
��2�����̹����У�298K��c(Mn2+)Ϊ1.05 mol/L-1ʱ��ʵ����MnCO3�IJ�������ҺpH����Ӧʱ��Ĺ�ϵ��ͼ��ʾ������ͼ����Ϣ�ó��Ľ����� ��
��3���ӳ��̹����еõ�����MnCO3�IJ��������ǣ����ˡ� ��
��4��Ϊ�ⶨij���̿��ж������̵�����������ȷ����1.20g���̿���Ʒ������2.68g�����ƹ��壬�ټ���������ϡ���Ტ����(���ʲ��μӷ�Ӧ)����ַ�Ӧ����ȴ����������Һת�Ƶ�250mL����ƿ��������ˮϡ�����̶ȣ�����ȡ��25.0mL����0.0200mol��L-1���������Һ���еζ���������20.0mL��Һʱǡ����ȫ��Ӧ��
��֪������ء��������������������¾��ܽ�������(Na2C2O4)������
2MnO4- + 5C2O42- + 16H+ == 2Mn2+ + 10CO2��+ 8H2O
MnO2 + C2O42- + 4H+ == Mn2+ + 2CO2��+ 2H2O
������̿��ж������̵��������� (д���������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ij��������Һ�м���������ˮ�������Կɴ����������
A��Fe3����K����SO42����NO3�� B��K����Na����SO32����Cl��
C��NH4+��K����SO42����Br�� D��K����Na����AlO2�� ��NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ϻ���ʮ��У������ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
һ�������ºϳ���ϩ6H2(g) �� 2CO2(g) 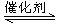 CH2��CH2(g) �� 4H2O(g)����֪�¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ������˵���������
CH2��CH2(g) �� 4H2O(g)����֪�¶ȶ�CO2��ƽ��ת���ʺʹ�����Ч�ʵ�Ӱ����ͼ������˵���������
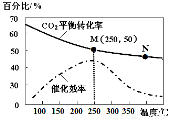
A��������ϩ�����ʣ�v(M)�п���С��v(N)
B��ƽ�ⳣ����KM ��KN
C���������ܻ�Ӱ��CO2��ƽ��ת����
D����Ͷ�ϱ�n(H2) : n(CO2)��3: 1����ͼ��M��ʱ����ϩ���������Ϊ7.7%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ�Թ��и����ϵ�һ����Ͽ������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ȷ��ʾ���з�Ӧ�����ӷ���ʽ��
A��Ũ��������м��Ӧ��2Fe+6H+=2Fe3++3H2��
B������CuSO4��Һ��Ӧ��2Na+Cu2+=Cu+2Na+
C��NaHCO3��Һ��ϡH2SO4��Ӧ��CO32һ+2H+=H2O+CO2��
D����������Һ�м������������������Һ��Al3++2SO42-+2Ba2++4OH-=2BaSO4+AlO2һ+2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���㽭ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йػ�ѧ���������ȷ����
A��H2O2�ĵ���ʽ��
B����������ķ���ʽ��SiO2
C��������ӵ����ģ�ͣ�
D�����ӽṹʾ��ͼ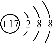 �����Ա�ʾ35Cl����Ҳ���Ա�ʾ37Cl��
�����Ա�ʾ35Cl����Ҳ���Ա�ʾ37Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�긣��ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��1����ӦFe(s)+CO2(g) FeO(s)+CO(g) ��H1��ƽ�ⳣ��ΪK1��
FeO(s)+CO(g) ��H1��ƽ�ⳣ��ΪK1��
��ӦFe(s)+H2O(g) FeO(s)+H2(g) ��H2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶�ʱK1��K2��ֵ���±���
FeO(s)+H2(g) ��H2��ƽ�ⳣ��ΪK2���ڲ�ͬ�¶�ʱK1��K2��ֵ���±���
700�� | 900�� | |
K1 | 1��47 | 2��15 |
K2 | 2��38 | 1��67 |
�ٷ�ӦCO2(g) + H2(g) CO(g) + H2O(g) ��H��ƽ�ⳣ��ΪK�����H= ���á�H1�͡�H2��ʾ����K= ����K1��K2��ʾ�����������������֪����ӦCO2(g) + H2(g)
CO(g) + H2O(g) ��H��ƽ�ⳣ��ΪK�����H= ���á�H1�͡�H2��ʾ����K= ����K1��K2��ʾ�����������������֪����ӦCO2(g) + H2(g) CO(g) + H2O(g)�� ��Ӧ������ȡ����ȡ�����
CO(g) + H2O(g)�� ��Ӧ������ȡ����ȡ�����
�����ж�CO2(g) + H2(g) CO(g) + H2O(g)�ﵽ��ѧƽ��״̬�������� ������ţ���
CO(g) + H2O(g)�ﵽ��ѧƽ��״̬�������� ������ţ���
A��������ѹǿ���� B�����������c(CO)����
C��v��(H2)= v��(H2O) D��c(CO)= c(CO2)
��2��һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬������ӦFe(s)+CO2(g) FeO(s)+CO(g) ��H > 0��CO2��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
FeO(s)+CO(g) ��H > 0��CO2��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
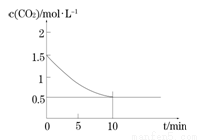
�� �������·�Ӧ��ƽ�ⳣ��Ϊ ��������������CO2����ʼŨ��Ϊ2.0 mol��L��1����ƽ��ʱCO2��Ũ��Ϊ____________mol��L��1��
�����д�ʩ����ʹƽ��ʱ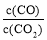 �������__________������ţ���
�������__________������ţ���
A�������¶� B������ѹǿ
C������һ������CO2 D���ټ���һ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�갲��ʡ��У��һ�ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ���ǣ� ��
A��Cl2ͨ��ˮ�У�Cl2+H2O�T2H++Cl��+ClO��
B��˫��ˮ�м���ϡ�����KI��Һ��H2O2+2H++2I���TI2+2H2O
C����ͭ���缫���CuSO4��Һ��2Cu2++2H2O 2Cu+O2��+4H+
2Cu+O2��+4H+
D��Na2S2O3��Һ�м���ϡ���2S2O32��+4H+�TSO42��+3S��+2H2O
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com