
| 元素代号 | X | Y | Z | M | R |
| 原子半径(×10-10m) | 1.60 | 1.86 | 0.75 | 0.74 | 1.02 |
| 主要化合价 | +2 | +1 | +5,-3 | -2 | +6,-2 |
| A. | Z的最高价氧化物对应的水化物与其最简单氢化物反应生成的化合物中含离子键和极性键 | |
| B. | 最简单氢化物的稳定性:Z>M | |
| C. | 最简单氢化物的沸点高低顺序为:R>M | |
| D. | 最高价氧化物对应水化物的碱性强弱顺序为:X>Y |
分析 短周期元素中,M、R都有-2价,处于ⅥA族元素,R有+6价,M无正价,且M的原子半径较大,则R为S元素、M为O元素;X、Y化合价分别为+2、+1价,则分别处于ⅡA族、IA族,且原子半径Y>X>硫,故X为Mg、Y为Na;Z有+5、-3价,处于ⅤA族,原子半径小于硫的,故Z为N元素,据此解答.
解答 解:短周期元素中,M、R都有-2价,处于ⅥA族元素,R有+6价,M无正价,且M的原子半径较大,则R为S元素、M为O元素;X、Y化合价分别为+2、+1价,则分别处于ⅡA族、IA族,且原子半径Y>X>硫,故X为Mg、Y为Na;Z有+5、-3价,处于ⅤA族,原子半径小于硫的,故Z为N元素.
A.Z的最高价氧化物对应的水化物与其最简单氢化物反应生成的化合物为硝酸铵,含离子键和极性键,故A正确;
B.非金属性M(O)>Z(N),故氢化物稳定性M(O)>Z(N),故B错误;
C.水分子之间存在氢键,沸点高于硫化氢的,故C错误;
D.金属性Na>Mg,故碱性:氢氧化钠>氢氧化镁,故D错误.
故选A.
点评 本题考查结构性质位置关系应用,根据化合价及原子半径推断元素是解题关键,注意对元素周期律的理解掌握,注意氢键对位置性质的影响.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案 名校联盟冲刺卷系列答案
名校联盟冲刺卷系列答案科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | B A D C E | B. | E C D A B | C. | A B E D C | D. | C D E B A |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向1mL 1mol/L NaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/L FeCl3溶液 |
| C | 除去甲烷中的乙烯 | 将混合气通入溴水洗气 |
| D | 探究温度对化学平衡的影响 | 将NO2球浸泡在冷、热水中,观察颜色的变化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素属于第七周期 | |
| B. | 该元素位于ⅢA 族 | |
| C. | 该元素为金属元素,性质与Pb相似 | |
| D. | 该同位家原子含有114个电子,184个中子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
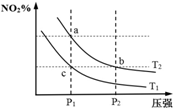 在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )
在密闭容器中发生反应N2O4(g)?2NO2(g)△H=+57kJ•mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示.下列说法正确的是( )| A. | 反应温度:T1>T2 | B. | b、c两点的反应速率:v(b)>v(c) | ||
| C. | a、c两点气体的颜色:a浅,c深 | D. | a、b两点的平衡常数:Kb>Ka |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | a和b不连接时,铁片上会有金属铜析出 | |
| B. | a和b用导线连接时,铜片上发生的反应为:Cu2++2e-═Cu | |
| C. | 无论a和b是否连接,铁片均会溶解,溶液均从蓝色逐渐变成浅绿色 | |
| D. | a和b连接时,铜片上发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com