
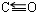 ;写出另一与CO互为等电子体的化学式CN-.
;写出另一与CO互为等电子体的化学式CN-.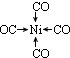 ;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.
;写出基态Ni原子的电子排布式1s22s22p63s23p63d84s2.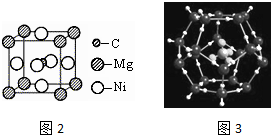
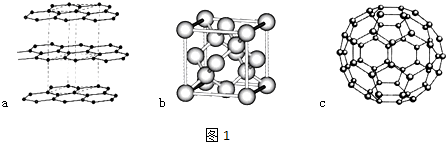
分析 (1)a为石墨,每个C原子价层电子对个数是3,根据价层电子对互斥理论判断C原子杂化类型,b为正四面体结构,则对应的物质是金刚石,c是C60的分子结构模型,平均每个C形成1.5个σ键;
(2)C60单质为分子晶体,微粒之间的作用力为分子间作用力,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1:3,则K3C60属于离子晶体;
(3)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,则C、O之间为三键;等电子体中原子数和价电子数都相同;
(4)根据配合物Ni(CO)4的Ni为中心原子,CO为配体表示Ni(CO)4 的结构,Ni元素是28号元素,根据核外电子排布规律书写基态原子的电子排布式;
(5)根据均摊法计算晶胞中各原子数目,进而确定化学式;电负性最大的即非金属性最强;
(6)键长越短键能越大;H2O分子间形成氢键.
解答 解:(1)a为石墨,每个C原子价层电子对个数是3,根据价层电子对互斥理论知C原子杂化类型为sp2;b为正四面体结构,则对应的物质是金刚石,c是C60的分子结构模型,平均每个C形成1.5个σ键,所以在每个C60分子中形成的σ键数目为60×1.5=90;
故答案为:sp2;金刚石; 90;
(2)C60单质为分子晶体,微粒之间的作用力为分子间作用力,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1:3,则K3C60属于离子晶体;故答案为:分子间作用力; 离子;
(3)CO分子中C原子上有一对孤对电子,C、O原子都符合8电子稳定结构,则CO的结构式为C≡O,等电子体中原子数和价电子数都相同,则 N2、CN-、CO的原子数都是2,价电子数都是10,则互为等电子体,故答案为:C≡O;CN-;
(4)配合物Ni(CO)4的Ni为中心原子,CO为配体,所以表示Ni(CO)4 的结构为 ;Ni元素是28号元素,位于第四周期第Ⅷ族,其基态原子的电子排布式1s22s22p63s23p63d84s2,故答案为:
;Ni元素是28号元素,位于第四周期第Ⅷ族,其基态原子的电子排布式1s22s22p63s23p63d84s2,故答案为: ,1s22s22p63s23p63d84s2;
,1s22s22p63s23p63d84s2;
(5)晶胞中N原子数目为1、Mg原子数目为8×$\frac{1}{8}$=1、Ni原子数目为6×$\frac{1}{2}$=3,故该晶体化学式为MgNi3N,电负性最大的即非金属性最强,所以C、Ni、Mg三种元素中,电负性最大的是C,故答案为:MgCNi3;C;
(6)因为键长越短键能越大,又O的半径小于C,所以共价键的键能H-O键>C-H键;又H2O分子间形成氢键,所以CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大;
故答案为:H-O键>C-H键;H2O分子之间形成氢键.
点评 本题是对物质结构的考查,为高频考点,涉及晶胞计算、分子结构、杂化轨道、配合物等,明确物质结构、分子结构及价层电子对互斥理论是解本题关键,注意配位键的表示方法,为易错点.


科目:高中化学 来源: 题型:解答题
 已知:在酸性条件下发生的反应为AsO43-+2I-+2H+═AsO33-+I2+H2O,在碱性条件下发 生的反应为AsO33-+I2+2OH-═AsO43-+H2O+2I-. 设计如图装置(C1、C2均为石墨电极),分别进行下述操作:
已知:在酸性条件下发生的反应为AsO43-+2I-+2H+═AsO33-+I2+H2O,在碱性条件下发 生的反应为AsO33-+I2+2OH-═AsO43-+H2O+2I-. 设计如图装置(C1、C2均为石墨电极),分别进行下述操作:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将过量CO2气体通入水玻璃中可制得硅酸和纯碱 | |
| B. | 标准状况下,2.24LCl2与过量稀NaOH溶液反应,转移电子0.1mol | |
| C. | 1L2mol•L-1明矾经水解可得到氢氧化铝胶体粒子数目为2×6.02×1023 | |
| D. | 漂白粉溶于水能导电,故漂白粉是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 4:3:2 | B. | 1:2:1 | C. | 2:1:1 | D. | 1:1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2Br在碱性溶液中水解 | |
| B. | 甲苯在催化剂(FeBr3)作用下与Br2发生苯环上的取代反应 | |
| C. |  与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 | |
| D. |  在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com