
【题目】下列说法不正确的是( )
A. 铵态氮肥和草木灰(含K2CO3)可混合施用 B. 明矾可做净水剂
C. 配制氯化铁溶液,常将氯化铁先溶于盐酸 D. 常将纯碱溶于热水中清洗油污
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有些垃圾可以用卫生填埋、焚烧、堆肥等方法处理。下列垃圾中,不适合用这样的方法处理的是( )
A.农作物垃圾,如秸秆等B.电池C.纸品D.纯棉纺织品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组为了深入探究二氧化硫的性质设计以下装置进行了实验。

步骤一:检验装置气密性后向B、C中各加入20mL图示液体。
步骤二:打开A中活塞,反应进行10分钟后关闭活塞。
步骤三:用pH计分别测量B、C试管中溶液的pH。
结合上述实验,回答以下问题:
请回答下列问题:
(1)装置A中盛放亚硫酸钠的仪器名称是________,其中发生反应的化学方程式为_______________________。
(2)甲同学认为两瓶中pH大致相等,原因是二氧化硫溶于水后生成了酸性物质_____________,该物质发生电离所致。
(3)通过pH计测定,B瓶中pH为2.13,C瓶中pH为1.05。为了解释该实验现象,该同学提出进行多次平行实验,目的是_______________________。
测定结果如下:
第1次实验 | 第2次实验 | 第3次实验 | |
B瓶中pH | 2.15 | 2.10 | 2.17 |
C瓶中pH | 1.10 | 1.12 | 1.09 |
实验发现:C瓶中溶液的酸性始终比B瓶中的酸性强。
(4)通过查阅文献,I﹣可以作为水溶液中SO2歧化反应的催化剂,可能的催化过程分两步进行如下,将ii补充完整。
i.SO2+4I﹣+4H+=S↓+2I2+2H2O
ii.I2+2H2O+___═___+___+2I﹣
(5)最终结论:C瓶中溶液酸性强于B瓶,是由于生成了____________,该过程中体现出二氧化硫哪些化学性质________________(选填“氧化性”,“还原性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 反应物的热效应与是否使用催化剂无关
B. 4NO2(g)+O2(g)=2N2O5 (g)的过程属于熵增加过程
C. 由C(石墨)= C(金刚石)△H﹥0,可知金刚石比石墨稳定
D. 对任何化学反应来说,反应速率越大,反应现象就越明显
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种气态烃的混和物共0.1mol,完全燃烧后得3.36L(标况下)CO2和3.6g水,下列说法正确的是( )
A. 一定有甲烷B. 一定有乙烯
C. 可能有乙烷D. 一定有乙烷,但不一定有甲烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4气体分子。N4分子结构如图所示,下列说法正确的是( )
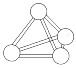
A. N4分子中只含有非极性键B. N4分子属于一种新型的化合物
C. 1 mol N4分子所含共价键数为4NAD. N4沸点比P4(白磷)高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)![]() COS(g)+H2(g)K=0.1,反应前CO物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
COS(g)+H2(g)K=0.1,反应前CO物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
A. 升高温度,H2S浓度增加,表明该反应是吸热反应 B. CO的平衡转化率为80%
C. 反应前H2S物质的量为7mol D. 通入CO后,正反应速率逐渐增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示构成细胞的元素、化合物及其作用,a、b、c、d代表不同的小分子物质,A,B,C代表不同的大分子物质,下列叙述错误的是( )

A. 在动物细胞内,与物质A作用最相近的物质是糖原
B. 若B代表的物质能降低血糖浓度,则与其合成、分泌密切相关的细胞器有核糖体和高尔基体等
C. b→B的生理过程完成的场所在核糖体,且有水的产生
D. a、b、c、d分别为葡萄糖、氨基酸、脱氧核苷酸和促性腺激素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某反应中的反应物和生成物有FeCl3、FeCl2、Cu、CuCl2。有人将上述反应设计成原电池。
(1)则该电池负极材料为:__________________,负极反应式为________________;
(2)正极材料为:_____________,该电池总的化学反应式为_______________;
(3)一段时间后负极质量减轻m g,则下列说法正确的是:________(填写序号)。
A.电路中通过的电子为m/32 mol
B.正极质量增加56m/64 g
C.原电池工作过程中电子由正极经导线流向负极
D.原电池工作过程中Cl向负极移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com