
| A.500 mL容量瓶 | B.胶头滴管 | C.试管 | D.托盘天平 |
科目:高中化学 来源:不详 题型:单选题
| A.萃取操作可在普通漏斗中完成 |
| B.浓烧碱液沾到皮肤上应立即用稀盐酸冲洗 |
| C.闻未知液体或气体的气味时,应该将试剂瓶口距离口鼻远一些,用手轻轻搧动。 |
| D.用容量瓶配制好一定浓度的某溶液后,将溶液保存在容量瓶中并贴上标签。 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.蒸馏液体时,冷水应从冷凝管的上端进入 |
| B.过滤时玻璃棒的末端应轻轻靠在三层的滤纸上 |
| C.萃取分液时,放出下层液体后,接着换一个新的烧杯放出上层液体 |
| D.称量NaOH固体,先在天平两盘上放大小相等纸片,然后NaOH放在左盘纸片上称量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用滤纸擦干净 | B.多次用水洗涤 |
| C.在酒精灯火焰上灼烧 | D.用稀盐酸洗涤,再灼烧到火焰呈无色为止 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 1.5 | 3.3 | 9.4 |
| 完全沉淀的pH | 3.7 | 5.2 | 11.0 |
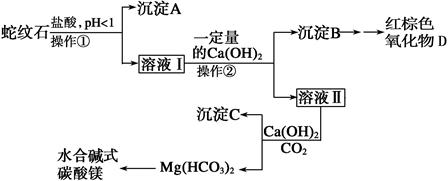
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com