
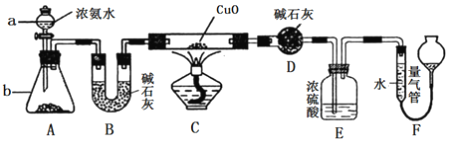
【题目】某课外活动小组欲利用CuO与NH3反应,研究NH3的某种性质并测定其组成,设计了如下实验装置(夹持装置未画出)进行实验。请回答下列问题:
(1)仪器a的名称为________;仪器b中可选择的试剂为________;
(2)实验室中利用下列各组物质,进行喷泉实验,不能成功的是(______)
A.Cl2与饱和食盐水 B.CO2 与40%的NaOH溶液
C.NH3与饱和食盐水 D.HCl与水
(3)实验中观察到装置C中黑色CuO粉末变为红色固体,量气管有无色无味的气体,上述现象证明NH3具有还原性,写出相应的化学方程式 _____________________.
(4)E装置中浓硫酸的作用_____________________
(5)实验完毕,若测得干燥管D增重mg,装置F测得气体的体积为nL(已折算成标准状况),则氨分子中氮、氢的原子个数比为_____________(用含m、n字母的代数式表示)
【答案】 分液漏斗 氧化钙或氢氧化钙或碱石灰 A 3CuO + 2NH3![]() 3Cu + N2↑ + 3H2O 吸收未反应的氨气,阻止F中水蒸气进入D 9n/11.2m
3Cu + N2↑ + 3H2O 吸收未反应的氨气,阻止F中水蒸气进入D 9n/11.2m
【解析】试题分析:(1)实验室中常用浓氨水加热或将浓氨水滴加到固体氧化钙或氢氧化钙上,利用氧化钙或氢氧化钙的吸水性及溶解放热来促使氨气溢出。(2)进行喷泉实验成功的关键是气体在液体中溶解度大。产生于外界足够大的压强差。Cl2在饱和食盐水溶解的少,不能形成压强差。进行喷泉实验,不能成功。其它选项都可以。(3)NH3和CuO加热时发生氧化还原反应的方程式是:3CuO + 2NH3![]() 3Cu + N2↑ + 3H2O(4)E装置中浓硫酸的作用是吸收未反应的氨气,阻止F中水蒸气进入D . (5)干燥管D增重mg,即吸收水蒸气的质量是mg,装置F测得气体的体积为nL,就是N2在标准状况体积是nL。n(H2O):n(N2)=(mg÷18g/mol):(nL÷22.4L/mol)="11.2m:9n." 则氨分子中氮、氢的原子个数比为(9n×2): (11.2m×2)= 9n/11.2m
3Cu + N2↑ + 3H2O(4)E装置中浓硫酸的作用是吸收未反应的氨气,阻止F中水蒸气进入D . (5)干燥管D增重mg,即吸收水蒸气的质量是mg,装置F测得气体的体积为nL,就是N2在标准状况体积是nL。n(H2O):n(N2)=(mg÷18g/mol):(nL÷22.4L/mol)="11.2m:9n." 则氨分子中氮、氢的原子个数比为(9n×2): (11.2m×2)= 9n/11.2m


科目:高中化学 来源: 题型:
【题目】糖类、油脂和蛋白质是维持人体生命活动的三大营养物质。下列有关说法正确的是
A. 三大营养物质均属于天然高分子化合物
B. 食用的蛋白质、糖和油脂都可发生水解反应
C. 糖类均有甜味,均易溶于水
D. 75%酒精常用于消毒是因为酒精使蛋白质变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为探究NH3的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题: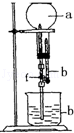
(1)写出实验室制取氨气的化学方程式 .
(2)要得到干燥的氨气可选用 作干燥剂.
A.碱石灰(CaO和NaOH的混合物)
B.浓硫酸
C.浓硝酸
D.氢氧化钠溶液
(3)用如图装置进行喷泉实验,烧瓶中已装满干燥氨气,引发水上喷的操作是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可用于测量阿伏加德罗常数的装置示意图,其中A是纯铜片、B是石墨,插在100 mL CuSO4稀溶液中,铜片、石墨与引出导线相连,引出端分别为X、Y。
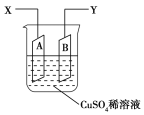
(1)当以I A的电流电解6 min后,测得铜片A质量减少2.56 g,则图装置中的X端应与直流电的________极相连。
(2)电解后将电源反接,2I A的电流电解6 min后,假设溶液体积不变,测得溶液中CuSO4物质的量浓度为0.1 mol/L,则原溶液中CuSO4物质的量浓度________mol/L。溶液中H+的物质的量浓度为________mol/L。
(3)列式计算实验测得阿伏加德罗常数NA(用I表示)________mol-1。(已知电子电量e=1.60×10-19 C)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NO2与N2O4可相互转化:2NO2(g)![]() N2O4(g) ΔH=-24.2 kJ·mol-1,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如下图所示。下列推理分析不合理的是( )
N2O4(g) ΔH=-24.2 kJ·mol-1,在恒温下,将一定量NO2和N2O4(g)的混合气体充入体积为2 L的密闭容器中,其中物质的量浓度随时间变化的关系如下图所示。下列推理分析不合理的是( )

A. 前10 min内,用v(NO2)表示的反应速率为0.04 mol·L-1·min-1
B. 反应进行到10 min时,体系放出的热量为9.68 kJ
C. a点正反应速率小于逆反应速率
D. 25 min时,正反应速率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中NO产生的反应为:N2(g)+O2(g)![]() 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始反应条件改变时N2的浓度随时间的变化。下列叙述正确的是:

A. 温度T下,该反应的平衡常数K=![]()
B. 温度T下,随着反应的进行,混合气体的密度减小
C. 曲线b对应的条件改变可能是加入了催化剂
D. 若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com