
工业上以锂辉石(Li2O·Al2O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
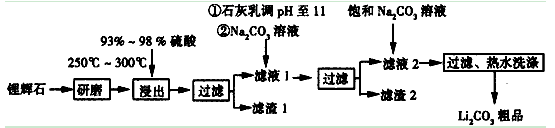
已知:①Li2O·Al2O3·4SiO2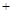 H2SO4(浓)
H2SO4(浓)  Li2SO4
Li2SO4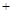 Al2O3·4SiO2·H2O↓
Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示:
|
T/℃ |
20 |
40 |
60 |
80 |
|
|
1.33 |
1.17 |
1.01 |
0.85 |
|
|
34.2 |
32.8 |
31.9 |
30.7 |
③从滤渣1中提取出Si的部分流程如下图所示:

根据以上信息,请回答下列问题:
(1)括号内应提供的相应条件和物质 、 。
(2)方框中所得物质的化学式 。
(3)使用浓硫酸并加热到250℃~300℃的目的是 。
(4)②处加Na2CO3溶液所发生反应的离子方程式 、 。
(5)滤渣2的主要成分有 。
(6)如何检验Li2CO3是否洗涤干净? 。
(1)加热或高温(1分) C和高温 (2分) (2) SiO2 (1分)
(3)减少杂质的溶解、提高Li2SO4的浸出率、加快浸出速率(每项1分,共2分,任意两项均得2分,其它合理答案也可)
(4) Ca2+ + CO32- = CaCO3↓(1分) CaSO4 + CO32- = CaCO3 + SO42- (2分)
(5) Mg(OH)2和CaCO3 (每个1分,共2分)
(6)取最后一次洗涤液少许于试管中,先在其中加入足量稀盐酸,然后滴入几滴BaCl2溶液,若未出现白色沉淀,则洗涤干净,反之则不干净。(其它合理答案也可,2分)
【解析】
试题分析:H4SiO4加热生成SiO2,SiO2与C在高温条件下反应生成单质Si和CO,所以(1)括号内相应条件和物质分别为加热、C和高温;(2)方框中物质为H4SiO4加热分解的产物:SiO2。
(3)使用浓硫酸并加热到250℃~300℃的目的是减少杂质的溶解、提高Li2SO4的浸出率、加快浸出速率。
(4)加入H2SO4后生成CaSO4,CaSO4微溶,含Ca2+和CaSO4固体,所以加入Na2CO3反应的离子方程式为:Ca2+ +CO32- =CaCO3↓、CaSO4+CO32- =CaCO3+SO42‾。
(5)加入Ca(OH)2和Na2CO3后,OH‾与溶液中的Mg2+反应,Ca2+与CO32‾反应,所以滤渣2的主要成分为Mg(OH)2和CaCO3。
(6)假如Li2CO3没有洗涤干净,表面会沾附Na2SO4溶液,所以用稀盐酸和BaCl2溶液进行检验。
考点:本题考查化学工艺流程的分析、离子方程式的书写、沉淀是否洗涤干净的方法。


科目:高中化学 来源:2013届山西省忻州一中高三第一次月考化学试卷(带解析) 题型:填空题
(12分)工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下: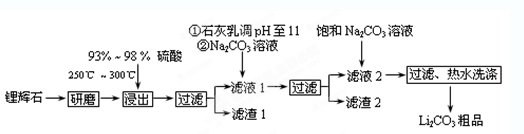
已知:①Li2O·Al2O3·4SiO2 +H2SO4(浓)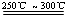 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓
②某些物质的溶解度(S)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
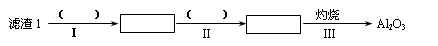
查看答案和解析>>
科目:高中化学 来源:2012-2013学年山西省高三第一次月考化学试卷(解析版) 题型:填空题
(12分)工业上以锂辉石(Li2O·A12O3·4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂。其部分工艺流程如下:
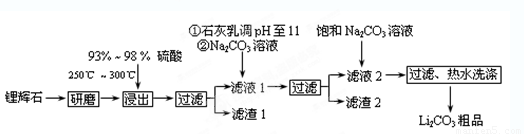
已知:① Li2O·Al2O3·4SiO2
+H2SO4(浓)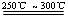 Li2SO4+Al2O3·4SiO2·H2O↓
Li2SO4+Al2O3·4SiO2·H2O↓
② 某些物质的溶解度(S)如下表所示。
|
T/℃ |
20 |
40 |
60 |
80 |
|
S(Li2CO3)/g |
1.33 |
1.17 |
1.01 |
0.85 |
|
S(Li2SO4)/g |
34.2 |
32.8 |
31.9 |
30.7 |
(1)从滤渣1中分离出Al2O3的部分流程如下图所示,括号表示加入的试剂,方框表示所得到的物质。则步骤Ⅱ中最佳反应的离子方程式是____________________________。
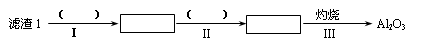
(2)已知滤液1中的主要离子为Li+、Mg2+、Ca2+、SO42-,滤渣2的主要成分有Mg(OH)2和CaCO3。向滤液1中加入石灰乳的作用是(运用化学平衡原理简述,并写离子方程式)
__________________________________________________________________。
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下。
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3。
① a中,阳极的电极反应式是______________________________________。
② b中,生成Li2CO3反应的化学方程式是______________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com