
海水是宝贵的自然资源,从海水中可以提取多种化工原料,如图是某工厂对海水综合利用的示意图:
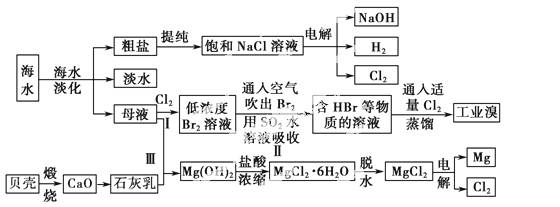
(1)在粗盐中含有Ca2+、Mg2+、SO等杂质,电解精制时所用的试剂有①盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。则加入试剂的先后顺序是____________(填编号)。
(2)工业上电解饱和食盐水的离子方程式:_________。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的是____________ _____。
_____。
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式:_____________________。
(4)从步骤Ⅲ得到的Mg(OH)2沉淀中混有少量的Ca(OH)2,除去少量Ca(OH)2的方法是向沉淀中加入________溶液,充分搅拌后经________(填操作方法)可得纯 净的Mg(OH)2。
净的Mg(OH)2。
(5)在制取无水氯化镁时需要在干燥的HCl气流中加热MgCl2·6H2O的原因:______________________。
(6)电解无水氯化镁所得的镁蒸气在特定的环境里冷却后即为固体镁,下列物质中可以用作镁蒸气冷却剂的是________(填序号)。
A.H2 B.CO2 C.空气 D.O2 E.水蒸气
科目:高中化学 来源: 题型:
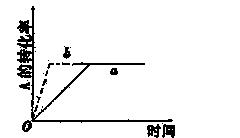
已知某可逆反应在密闭容器中进行:A(g)+2B(g) 3C(g)+D(g)(正反应为放热反应)。下图中曲线a代表一定条件下该反应的过程,若使曲线a变为b曲线,可采取的措施是
( )
A、增大A的浓度 B、缩小容器的体积 C、加入催化剂 D、升高温度
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、G五种元素分属三个短 周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
(1) Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是
(写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3) Y、G的单质或两元素之间形成的化合物可作水消毒剂的有
(写出其中两种物质的化学式)。
(4)X2M的燃烧热ΔH=-a kJ·mol-1,写出X2M燃烧反应的热
化学方程式:  。
。
(5)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
(6) 熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如右),反应原
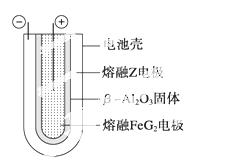
理为2Z+FeG2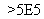 Fe+2ZG
Fe+2ZG
放电时,电池的正极反应式为  ;
;
充电时, (写物质名称)电极接电源的负极;该电池的电解质为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,错误的是
A. 钢铁腐蚀时可能发生的正极反应:2H2O+ O2+ 4e- =4OH一
=4OH一
B. 明矾水解的离子方程式: Al3++3 H2O Al(OH)3+3H+
Al(OH)3+3H+
C.少量氢氧化钙溶液与碳酸氢钠溶液混合:OH-+ HCO3一=H2O+ CO32-
D. 表示氢气燃烧的热化学方程式2H2(g)+O2(g)=2H2O(l);△H=+571.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语。
下列有关化学用语的表示方法中正确的是( )
A.H2O2的电子式: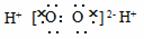
B.NH4I的电子式 : 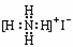
C.原子核内有8个中子的碳原子: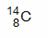
D.CO2分子的结构式:O=C=O
查看答案和解析>>
科目:高中化学 来源: 题型:
钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在________部分发生反应,在________部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为:_____________;
加入硅、锰和铝的目的是____________。
(3)不锈钢含有的 Cr 元素是在炼钢过程的氧吹________(填“前”或“后”)加入,原因是_________________。
(4)炼铁和炼钢生产中,尾气均含有的主要污染物是________。从环保和经济角度考虑,上述尾气经处理可用作_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品。
回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾、溴、镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是Br2+Na2CO3+H2O 
 NaBr + N
NaBr + N aBrO3+NaHCO3,吸收1mol Br2时,转移的电子数为 mol。
aBrO3+NaHCO3,吸收1mol Br2时,转移的电子数为 mol。
(3)海水提镁的一段工艺流程如下图:
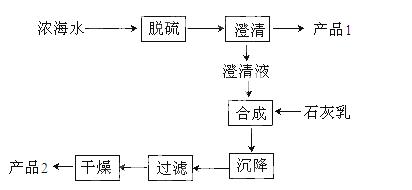
浓海水的主要成分如下:
| 离子 | N | Mg2+ | Cl- | SO42- |
| 浓度/g/L | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品2的化学式为 ,1L浓海水最多可得到产 品2的质量为 g。
品2的质量为 g。
(4)采用石墨阳极、不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
由黄铜矿(主要成分是CuFeS2) 炼制精铜的工艺流程示意图如下:
炼制精铜的工艺流程示意图如下:
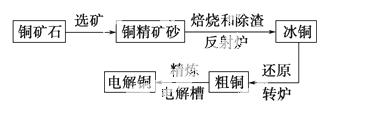
(1)在反射炉中,把铜精矿砂和石英砂混合加热到1 000 ℃左右,黄铜矿与空气反应生成Cu和Fe的低价硫化物,且部分Fe的硫化物转变为低价氧化物。该过程中两个主要反应的化学方程式分别是____________________、__________________________,反射炉内生成 炉渣的主要成分是________;
炉渣的主要成分是________;
(2)冰铜(Cu2S和FeS互相熔合而成)含Cu量为20%~50%。转炉中,将冰铜加熔剂(石英砂)在1 200 ℃左右吹入空气进行吹炼。冰铜中的Cu2S被氧化成Cu2O,生成的Cu2O与Cu2S反应,生成含Cu量约为98.5%的粗铜,该过程发生反应的化学方程式分别是____________;
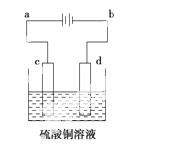
(3)粗铜的电解精炼如右图所示。在粗铜的电解过程中,粗铜板应是图中电极________(填图中的字母);在电极d上发生的电极反应式为____________________________;若粗铜中还含有Au、Ag、Fe,它们在电解槽中的存在形式和位置为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有X、Y、Z、W四种含14个电子的粒子,其结构特点如下:
| 粒子代码 | X | Y | Z | W |
| 原子核数 | 单核 | 不同元素构成的两核 | 同元素构成的两核 | 同元素构成的两核 |
| 粒子的电荷数 | 0 | 0 | 两个负电荷 | 0 |
(1)A原子核外比X原子多3个电子,A的原子结构示意图是____________,X的氧化物晶体中含有化学键类型是____________,含1 mol X的氧化物晶体中含有共价键数目为________。
(2)Z与钙离子组成的化合物的电子式为_________________,
其晶体类型为____________。
(3)14 g Y完全燃烧放出的热量是141.5 kJ,写出Y燃烧的热化学方程式______________________。
(4)组成W的元素最高价氧化物对应的水化物甲有下图所示转化关系(反应条件和其他物质已略)



①写出丁在高温下与水蒸气反应的化学方程式________________________。
②组成W的元素的简单氢化物极易溶于水的主要原因是
______________________,该氢化物与空气可以构成一种燃料电池,电解质溶液是KOH溶液,其负极的电极反应式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com