
��8�֣���ϡ������μ���ʢ�������Ͻ�������У�������ǡ����ȫ�ܽ�ʱ��������״����NO 40.32L������Ӧ�����Һƽ���ֳ����ȷݣ��ֱ��������ʵ�飺
��1����һ����Һ����μ���2 mol��L-1NaOH��Һ����ǡ�ôﵽ�������������ǿ�����O2���������������NaOH��Һ�����Ϊ________________��
��2���ڶ�����Һ�б���NaOH��Һ�����ڿ����г�ֽ��裬��ǡ�ôﵽ�����������������ij������ˡ�ϴ�ӡ���������ȵ�һ����5.1g����ù���������O2�����ʵ���Ϊ_______________��
��3����������Һ����μ���4 mol��L-1NaOH��Һ����Al(OH)3����ǡ���ܽ⣬����NaOH��Һ500mL������ԭ�Ͻ���������������д��������̣�(4��)
��1��900mL��0.9L (2��) ��2��0.075mol(2��)
��3������Naԭ���غ��У�n(NaOH)=n(NaAlO2)+n(NaNO3)
n(NaOH)=4mol/L��0.5L��3=6mol (1��)
�������������,n(HNO3)=4n(NO)=4��(40.32L/22.4L/mol)=7.2mol
��n(NaNO3)=3/4��7.2mol=5.4mol (1��)
n(Al)= n(NaAlO2)=" n(NaOH)" ��n(NaNO3)=6mol��5.4mol=0.6mol (1��)
m(Al)=0.6mol��27g/mol=16.2g (1��)
ԭ�Ͻ��к���������Ϊ16.2g ��������ѧ�����5.4g���ɵ�3�֣�
���������������1���������з�����ӦFe+4HNO3=Fe(NO3)3+NO+2H2O
Al+4HNO3=Al(NO3)3+NO+2H2O
Fe(NO3)3+3 NaOH= Fe(OH)3+3NaNO3
Al(NO3)3+3 NaOH= Al(OH)3+3NaNO3
���п��ܷ�����Fe+2 Fe(NO3)3= 3Fe(NO3)2
Fe(NO3)2+2NaOH= Fe(OH)2+2NaNO3
���������������ÿ����Һ��n(HNO3)="4n(NO)" ��1/3="4��(40.32L/22.4L/mol)" 1/3
=2.4mol
����NԪ���غ㣺n(HNO3)= n(NaNO3)+ n(NO)
��n(NO)="40.32L/(22.4L/" mol) ��1/3="0.6" mol
n(NaNO3)="1.8" mol
�� V��NaOH��=" 1.8" mol/2 mol��L-1 = 0.9L
��2���ڶ�����Һ�м���NaOH��Һ��ͬʱ�ڿ����г�ֽ��裬��ʱ��Fe(OH)2��ȫת��ΪFe(OH)3��������Ӧ 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3���ʳ������ص�������4Fe(OH)2���յ�������ˮ����������
4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3 ��m
32 68
n(O2) ��32g/ mol 5.1g
n(O2)= 0.075mol
���㣺��������������ϡ���ᷴӦΪ���壬�������ڴ˹����з����Ļ�ѧ��Ӧ���������л�ѧ���������á�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���������Ҫ�ɷ���Al2O3��Fe2O3��SiO2�ȣ���������ұ��Al2O3���������£�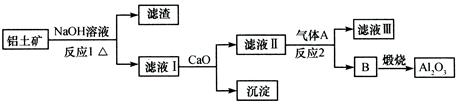
����˵����ȷ����
| A������Aһ��ΪHCl | B����Һ�������ʽ���NaAlO2 |
| C����������Ҫ�ɷ�Ϊ����� | D����Ӧ1����Ӧ2������������ԭ��Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��9�֣�����ʯ����Ҫ�ɷ���K2SO4��Al2(SO4)3��2Al2O3��6H2O��������������
��������ʯ�Ʊ�K2SO4�Ĺ�������������ʾ��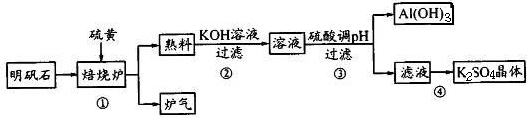
��1������¯�з������·�Ӧ�����ڷ���ʽ�б�ʾ������ת�Ƶķ������Ŀ
2Al2(SO4)3��3S 2Al2O3��9SO2��
2Al2O3��9SO2��
��2��������漰Al2O3�����ӷ���ʽΪ____��
��3������۵�pH����AI{OH)�������ӷ���ʽΪ____��������CO2����pH��������
.
��4������ܵ���Ҫ����������___ _�����ˡ�ϴ�Ӻ���
��5��¯�����տ���������;�����һ����__ _��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
A.��B��C��D��E��F�������ʵ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ֲ���δ���)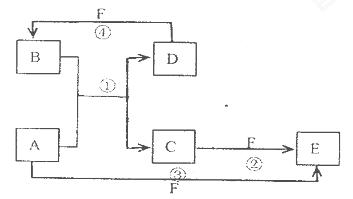
��1����AΪ�����ڽ������ʣ�DΪ�����ڷǽ������ʣ�������Ԫ�ص�ԭ������A��D��2��������Ԫ�ص�ԭ������������D��A��2����F��Ũ��Һ��A D��Ӧ���к���ɫ�������ɣ���AΪ___________________��
��Ӧ�ܵĻ�ѧ����ʽΪ____________________________________.
��2����AΪ�����Ľ������ʣ�D F����̬���ʣ���Ӧ����ˮ��Һ�н��У���Ӧ�ڣ���ˮ��Һ�н��У������ӷ���ʽ��____________________________.
��3����A��D��F���Ƕ����ڷǽ���Ԫ�ص��ʣ���A��D����Ԫ��ͬ���壬A��F����Ԫ��ͬ���ڣ���Ӧ�ٵĻ�ѧ����ʽΪ________________________.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��16�֣���ͭ����ұ��ͭ����Ҫԭ�ϡ�
��1����ҵ��ұ����ͭ��ij�ַ�ӦΪ��Cu2S+O2��2Cu+SO2
�ٵ����������11.2L����ʱ��ת�Ƶ�����ĿΪ ��
�ڽ���ͭ���е�⾫������ͭӦ�����Դ�� ����ӣ�������ij�ֽ�������п�Ĵ�ͭ��ͨ��һ��ʱ�������������ag���������Һ����bg�����ͭ�к�п����������Ϊ ��
��2������ͭ�����̿������´����������Ƶü�ʽ̼��ͭ��
��ͭ���ʷ����ڳ�ʪ�����У��������ɼ�ʽ̼��ͭ����Ӧ��ѧ����ʽ�� ��
�ڲ�����У�̼����鱗��뷴Ӧ�����ӷ���ʽΪ ��
�۲�����з�������3����Ӧ����֪��Ӧi)�����ɵ�������������á���д����Ӧiii)�Ļ�ѧ����ʽ��
i)Fe2O3+3H2SO4 ��Fe2(SO4)3+3H2O
ii) Cu2S+ Fe2(SO4)3 ��CuSO4+CuS+2FeSO4
iii)
�ܲ�����е���pH�����Һ�У�ͭ����Ũ������ܳ��� mol/L��
����֪Ksp[(Cu(OH)2)]��2��10��a��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��������Ϊһ�����ʹ��ܵ�أ���Ӧ���õ����Ӻͷ�չ��
��1��Al(NO3)3���Ʊ������ز�����ԭ��֮һ������Al(NO3)3�������ջ����е�ˮ�֣���Ҫ������ж������������岽������ͼ��ʾ��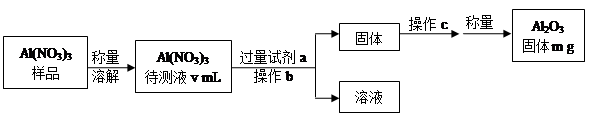
�ټ����Լ�a������Ӧ�����ӷ���ʽΪ ��
�ڲ���bΪ ������cΪ ��
��Al(NO3)3����Һ�У�c (Al3+) = mol��L-1����m��v��ʾ����
��2�������������ڽ����ơ�������Ͷ����ƣ�Na2Sx���ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մɣ��ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ������ͼ��ʾ��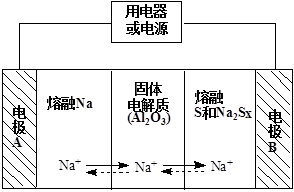
�ٸ����±����ݣ������жϸõ�ع����������¶�Ӧ������ ��Χ�ڣ�����ĸ��ţ���
| ���� | Na | S | Al2O3 |
| �۵�/�� | 97��8 | 115 | 2050 |
| �е�/�� | 892 | 444��6 | 2980 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
þ����Ͻ���һ����;�ܹ�Ľ������ϣ�Ŀǰ������60%��þ�ǴӺ�ˮ����ȡ�ġ�ijѧУ������ȤС��Ӻ�ˮɹ�κ����±(��Ҫ��Na����Mg2����Cl����Br����)��ģ�ҵ��������ȡþ����Ҫ�������£�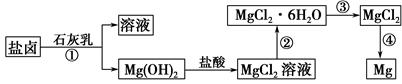
�ش��������⣺
(1)��ҵ�ϴ���±�л�ȡMg(OH)2��ʯ���������NaOH��Һ��ԭ���� ��
(2)�ӹ��̢ٵõ���Mg(OH)2�����л���������Ca(OH)2����ȥ����Ca(OH)2�ķ������Ƚ��������뵽ʢ�� ��Һ���ձ��У���ֽ���� �� (���������)�ɵô�����Mg(OH)2��
(3)��ͼ�Ǹ���ȤС����ƽ��й��̢۵�ʵ��װ��ͼ��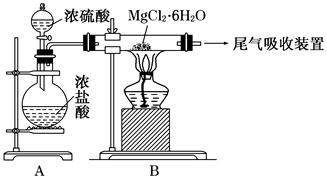
����װ��A�������� ��
(4)д�����̢��з�����Ӧ�Ļ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com