
科目:高中化学 来源:2016届湖北省高三普通班8月月考化学试卷(解析版) 题型:选择题
物质 R2CO3 的饱和溶液 V mL,密度为 ρ g·cm-3 ,c(R+) = P mol·L-1 ,溶质的质量分数为 a% ,溶质的相对分子量为 M,溶质的溶解度为sg。则下列表达式正确的是
A.a = 
B.s = 
C.P =  ×2
×2
D.V×ρ×a% = 
查看答案和解析>>
科目:高中化学 来源:2016届辽宁省大连市高三期初考试化学试卷(解析版) 题型:选择题
化合物A(C4H8Br2)可由下列反应制得,则C4H8Br2的结构式不可能的是
C4H10O C4H8
C4H8 C4H8Br2,
C4H8Br2,
A.CH3CH2CHBrCH2Br B.CH3CH(CH2Br)2
C.CH3CHBrCHBrCH3 D.(CH3)2CBrCH2Br
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g)反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2)/ mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
下列说法正确的是
A.反应在0~2min内的平均速率为v(SO2)=0.6 mol·L-1·min-1
B.反应在2~4min内容器内气体的密度没有变化
C.若升高温度,反应的平衡常数变为1.00,则正反应为放热反应
D.保持其他条件不变,起始时向容器中充入1.00mol MgSO4和1.00molCO,到达平衡时n(CO2)>0.60mol
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期开学考试化学试卷(解析版) 题型:选择题
下列做法不符合低碳发展原则的是
A.发展氢能和太阳能 B.限制塑料制品的使用
C.提高原子利用率,发展绿色化学 D.尽量用纯液态有机物代替水作溶剂
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省平凉市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
在下列实验操作中均用到的仪器是
①配制一定物质的量浓度的溶液;②用pH试纸检验溶液酸碱度;③过滤;④蒸发
A.试管 B.漏斗
C.胶头滴管 D.玻璃棒
查看答案和解析>>
科目:高中化学 来源:2016届安徽省高三摸底联考化学试卷(解析版) 题型:填空题
(14分)甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
回答下列问题:
(1)已知△H1=-99kJ·mol-1 ,△H3=+41kJ·mol-1,则△H2= kJ·mol-1。
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
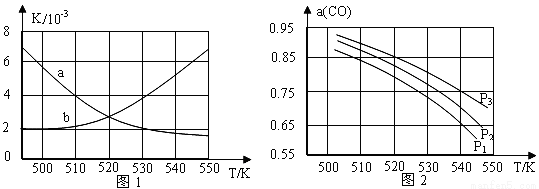
(3)若开始各气体的物质的量一定时,体系中的CO平衡转化率(α)与温度和压强的关系如图2所示。则α(CO)值随温度升高而 (填“增大”或“减小”);图2中的压强由大到小为 ,其判断理由是 。
查看答案和解析>>
科目:高中化学 来源:2016届山东省枣庄市高三9月阶段性学情检测化学试卷(解析版) 题型:选择题
对下列物质用途的解释不正确的是
A | B | C | D | |
用途 | 抗坏血酸(Vc)可作抗氧化剂 | 明矾可用于净水 | 纯碱可去油污 | “84”消毒液可用于漂白 |
解释 | Vc具有酸性 | 明矾在水中生成的氢氧化铝胶体具有吸附性 | 纯碱水解呈碱性 | 置于空气中生成的次氯酸有强氧化性 |
查看答案和解析>>
科目:高中化学 来源:2016届江西省高三上学期第一次月考化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-
B.NaHCO3溶液中:K+、Al3+、Cl-、SO42-
C.通入足量CO2的溶液:H+、NH4+、Al3+、SO42-
D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com