
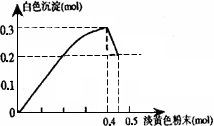
有一透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、![]() ,加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4 mol淡黄色粉末时,产生气体0.3 mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如下图所示:根据题意同答下列问题:
,加入一种淡黄色粉末状固体时,加热有刺激性气味的混合气体放出,同时生成白色沉淀.当加入0.4 mol淡黄色粉末时,产生气体0.3 mol,继续加入淡黄色粉末时,产生无刺激性气味的气体,且加入淡黄色粉末时产生白色沉淀的量如下图所示:根据题意同答下列问题:
(1)淡黄色粉末为________(填名称)
(2)溶液中肯定有________离子,肯定没有________.
(3)溶液中离子的物质的量之比为________
(4)写出下列方程式:
①淡黄色粉末与水反应的化学方程式:________________________
②产生刺激性气味气体的离子方程式:________________________
③沉淀部分减少时的离子方程式:____________________________
科目:高中化学 来源: 题型:阅读理解
| 实验步骤 | 实验现象 |
| (1)取少量该溶液,测定溶液pH | pH=0 |
| (2)取少量该溶液加热浓缩,加Cu片和浓 H2SO4,加热 | 有无色气体产生,气体遇空气变成红棕色 |
| (3)取少量该溶液,加少量BaCl2溶液 | 有白色沉淀 |
| (4)取(3)中上层清液,加足量AgNO3溶液 | 有白色沉淀,且不溶于稀HNO3 |
| (5)取少量该溶液,加NaOH溶液 | 有白色沉淀,NaOH过量时沉淀部分溶解 |
查看答案和解析>>
科目:高中化学 来源:湖北省黄冈中学2012届高三上学期期中考试化学试题 题型:022
有一无色透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量关系如图所示,请回答:

(1)淡黄色粉末为________(填名称).其电子式为________.
(2)溶液中肯定没有________离子.
(3)溶液中离子的物质的量之比为________.
(4)①淡黄色粉末与水反应的化学方程式为________,②沉淀部分减少时的离子方程式为________.
查看答案和解析>>
科目:高中化学 来源:2012届湖北省黄冈中学高三上学期期中考试化学试卷 题型:填空题
(7分)有一无色透明溶液,已知其中可能含有Fe3+、Mg2+、Cu2+、Al3+、NH4+,加入一种淡黄色粉末并加热,产生沉淀或气体的物质的量与淡黄色粉末的物质的量关系如图所示,请回答:
(1)淡黄色粉末为_____________(填名称)。其电子式为_____________
(2)溶液中肯定没有_____________离子。
(3)溶液中离子的物质的量之比为____________________________。
(4)①淡黄色粉末与水反应的化学方程式为_______ ___________,
②沉淀部分减少时的离子方程式为_________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省资阳市高二下学期期末考试化学试卷(带解析) 题型:实验题
(18分)透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶,制备它的一种配方中含有下列三种物质
甲 乙 丙
(1)下列试剂能与甲反应而褪色的是(填序号) 。
①溴的CCl4溶液 ②酸性KMnO4溶液 ③石蕊试液 ④含酚酞的烧碱溶液 ⑤FeCl3溶液
写出由甲在稀硫酸作用下水解的化学反应方程式:
(2)乙可以由淀粉通过下列转化制得(其中A、B、C、D均为有机物):
i.上述转化过程中涉及的条件X是 。
ii.物质A常用新制Cu(OH)2来检验,其主要的反应原理用化学方程式可表示为:
iii.上述转化过程中属于水解反应类型的有 个。
iv.D是一种液态卤代烃,已知其密度为ρ g/cm3为测定其相对分子质量,拟实验步骤如下:
第一步:准确量取该卤代烃V mL;
第二步:在锥形瓶中加入过量的稀NaOH溶液,塞上连有长玻璃管的塞子,加热;
第三步:反应完成后冷却溶液,加稀HNO3酸化;
第四步:滴加过量AgNO3溶液得浅黄色沉淀;
第五步:过滤,洗涤,干燥称重得固体m克。请回答:
a.该卤代烃中所含官能团的名称是 。
b.该卤代烃的相对分子质量用含ρ、V、m的代数式可表示为 。
c.如果在第三步中加入稀HNO3的量不足,则测得相对分子质量将 (填“偏大”,“偏小”或“无影响”)。
d.写出D→乙的化学反应方程式:
(3)化合物丙中含氧为29.09%,相对分子质量不超过120,在空气中完全燃烧时,只生成CO2和H2O,经实验检测得知丙还具有下列结构和性质特点:
①核磁共振氢谱检测只有两种吸收峰,且峰面积之比1∶2;
②与FeCl3溶液作用显紫色。
写出丙与Na2CO3反应的化学方程式:
查看答案和解析>>
科目:高中化学 来源:2013届四川省资阳市高二下学期期末考试化学试卷(解析版) 题型:实验题
(18分)透明聚酯玻璃钢可用于制造导弹的雷达罩和宇航员使用的氧气瓶,制备它的一种配方中含有下列三种物质

甲 乙 丙
(1)下列试剂能与甲反应而褪色的是(填序号) 。
①溴的CCl4溶液 ②酸性KMnO4溶液 ③石蕊试液 ④含酚酞的烧碱溶液 ⑤FeCl3溶液
写出由甲在稀硫酸作用下水解的化学反应方程式:
(2)乙可以由淀粉通过下列转化制得(其中A、B、C、D均为有机物):

i.上述转化过程中涉及的条件X是 。
ii.物质A常用新制Cu(OH)2来检验,其主要的反应原理用化学方程式可表示为:
iii.上述转化过程中属于水解反应类型的有 个。
iv.D是一种液态卤代烃,已知其密度为ρ g/cm3 为测定其相对分子质量,拟实验步骤如下:
第一步:准确量取该卤代烃V mL;
第二步:在锥形瓶中加入过量的稀NaOH溶液,塞上连有长玻璃管的塞子,加热;
第三步:反应完成后冷却溶液,加稀HNO3酸化;
第四步:滴加过量AgNO3溶液得浅黄色沉淀;
第五步:过滤,洗涤,干燥称重得固体m克。请回答:
a.该卤代烃中所含官能团的名称是 。
b.该卤代烃的相对分子质量用含ρ、V、m的代数式可表示为 。
c.如果在第三步中加入稀HNO3的量不足,则测得相对分子质量将 (填“偏大”,“偏小”或“无影响”)。
d.写出D→乙的化学反应方程式:
(3)化合物丙中含氧为29.09%,相对分子质量不超过120,在空气中完全燃烧时,只生成CO2和H2O,经实验检测得知丙还具有下列结构和性质特点:
①核磁共振氢谱检测只有两种吸收峰,且峰面积之比1∶2;
②与FeCl3溶液作用显紫色。
写出丙与Na2CO3反应的化学方程式:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com