
【题目】如图为以Pt为电极的氢氧燃料电池的工作原理示意图,稀H2SO4溶液为电解质溶液。下列有关说法不正确的是

A. a极为负极,电子由a极经外电路流向b极
B. a极的电极反应式:H2-2e-===2H+
C. 电池工作一段时间后,装置中c(H2SO4)增大
D. 若将H2改为CH4,消耗等物质的量的CH4时,O2的用量增多
科目:高中化学 来源: 题型:
【题目】A—E五种物质都含有同一种元素,它们之间的转化关系如图所示,其中A为淡黄色固体化合物,B为单质。

(1)固体A的名称为____,单质B的常见用途有:_____(任写一条)。
(2)写出下列反应的化学方程式
①B→C__________
②A→D__________
(3)写出将氯气通入C溶液中的化学方程式_____,其溶液有漂白作用,漂白原理是______。(写反应方程式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是有关钠与水反应及产物检验的实验装置。实验开始时先向管内加入滴有酚酞试液的水,使水位达到B端管口,然后迅速塞紧橡胶塞并拔掉大头针,此时Na掉入水中。回答下列问题:
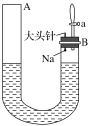
(1)钠与水反应的化学方程式为_____________。
(2)钠与水反应的现象有很多,不同的现象证明不同的性质。
①能证明钠的密度比水小的现象是_________。
②能证明钠的熔点低的现象是_________。
③能证明有氢氧化钠生成的现象是__________。
④能证明有气体产生的现象是A端液面________(填“上升”“下降”或“不变”,下同),B端液面________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某制糖厂以甘蔗为原料制糖,同时得到大量甘蔗渣,对甘蔗渣进行综合利用,可以提高经济效益,减少对环境的污染。如图所示为用甘蔗渣为原料制取各物质的转化过程图。
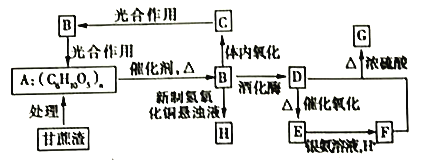
已知:①B在人体组织中发生缓慢氧化,放出热量,提供生命活动需要的能量。
②G是具有果香气味的液体,体积分数75%的D的水溶液常用于医疗消毒,并且可以代替汽油作汽车燃料。
③R—CHO![]() R—COOH
R—COOH
(1)A的化学名称为___________,B的分子式为___________。
(2)E的结构简式为___________,F分子中含有的官能团的名称为___________。
(3)D+F→G的化学方程式为___________,该反应的反应类型为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO43-+2I-+2H+ ![]() AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。
AsO33-+I2+H2O”设计成的原电池装置,其中C1、C2均为碳棒。甲组向图Ⅰ烧杯中逐滴加入适量浓盐酸;乙组向图ⅡB烧杯中逐滴加入适量40% NaOH溶液。


下列叙述中正确的是
A. 甲组操作时,电流表(A)指针发生偏转
B. 甲组操作时,溶液颜色变浅
C. 乙组操作时,C2作正极
D. 乙组操作时,C1上发生的电极反应为I2+2e-=2I-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起。工业级NaN3的制备分两步进行,反应的化学方程式如下:
i. 2Na +2NH3![]() 2NaNH2+ H2 ii. NaNH2+ N2O
2NaNH2+ H2 ii. NaNH2+ N2O![]() NaN3+H2O
NaN3+H2O
实验室利用如下装置模拟工业级NaN3的制备。
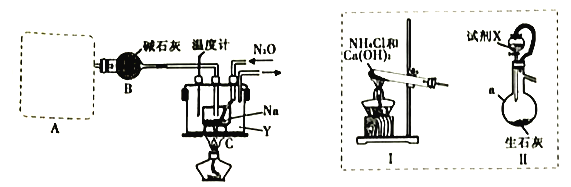
(1)装置A用于制取NH3,右图装置I和Ⅱ为气体发生装置。若选用装置I,则发生反应的化学方程式为_________________________________;若选用装置Ⅱ,则试剂X是___________(填试剂名称),仪器a的名称是___________。
(2)装置B的作用是_______________________________________________________。
(3)加热前需要先往装置C中通一段时间NH3的目的是______________________________。
(4)当观察到装置C中熔融钠单质的银白色光泽全部消失时,停止通氨气,开始通入N2O。装置C中的Y为___________(填字母)。
A.冷水浴 B.热水浴 C油浴
(5)该实验装置的缺陷是_________________________________(任写一点)。
(6)反应完全结束后,取出装置C中的混合物先后经加水、加乙醇、过滤、洗涤、干燥等操作得到NaN3固体,其中洗涤操作可用乙醚洗涤NaN3固体的原因___________。
(7)实验室用滴定法测定叠氮化钠产品中NaN3的质量分数:
操作方法:取2.500g产品配制成500.0mL溶液。取25.00mL溶液置于锥形瓶中,加入25.00mL0.1010mol·L-1(NH4)Ce(NO3)6溶液。充分反应后,稍稀释,加入4mL浓硫酸,滴入邻菲罗啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗(NH4)2Fe(SO4)2标准溶液的体积为14.80mL。
测定过程发生反应的方程式为:
2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑
Ce4++Fe2+=Ce3++Fe3+。
产品中NaN3的质量分数为___________%(保留1位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于苯乙烯(![]() )有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
)有下列叙述:① 能使酸性KMnO4溶液褪色;② 能使溴的四氯化碳溶液褪色;③ 可溶于水;④ 可溶于苯中;⑤ 能与浓硝酸发生取代反应;⑥ 所有的原子可能共平面。其中正确的是( )
A. ①②③④⑤ B. ①②⑤⑥ C. ①②④⑤⑥ D. 全部正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨在一定条件下发生如下反应:![]() ,当进入合成塔的
,当进入合成塔的![]() 和
和![]() 的体积比为1:3时,经测定,在一定温度、压强和催化剂条件下所得氨的平衡浓度(体积分数)如下表所示:
的体积比为1:3时,经测定,在一定温度、压强和催化剂条件下所得氨的平衡浓度(体积分数)如下表所示:
20MPa | 50MPa | |
500℃ | 19.1 | 42.2 |
而实际从合成塔出来的混合气体中含有氨约15%。
完成下列填空:
(1)目前公认的合成氨工业最恰当的催化剂是________。
a.酶 b.二氧化锰 c.铁触媒 d.五氧化二钒
(2)298K时合成氨,每生成![]() ,同时放出46.2kJ的热量。则该反应的热化学方程式为__________;该温度下,取
,同时放出46.2kJ的热量。则该反应的热化学方程式为__________;该温度下,取![]() 和
和![]() 放在一密闭容器中,在催化剂条件下反应,测得反应放出的热量总小于92.4kJ,其原因是________________________________。
放在一密闭容器中,在催化剂条件下反应,测得反应放出的热量总小于92.4kJ,其原因是________________________________。
(3)合成氨的温度和压强通常控制在约500℃以及20-50MPa的原因是_________________________________。
(4)实际上从合成塔出来的混合气体中氨的体积分数小于理论值的原因是________。
a.表中所测数据有明显误差 b.生成条件控制不当
c.氨的分解速率大于预测值 d.合成塔中的反应未达到平衡
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com