
| A.过量①与②分别与少量的锌(大小相同)反应时,开始时刻速率相同,反应中速率:①<② |
| B.将②、③两种溶液混合后,若呈中性,则消耗溶液的体积:②>③ |
| C.等体积的①、②、④溶液分别与足量铝粉反应,生成H2的量:②最大 |
| D.将③稀释a倍,将④稀释b倍,两溶液pH相等,则a<b倍 |
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 H+(溶液)+In-(溶液)
H+(溶液)+In-(溶液)| A.②⑤⑥ | B.①④ | C.①④⑤ | D.②③⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,把pH=2的亚硝酸溶液稀释100倍后pH=3.5 |
| B.常温下,0.1mol/L的亚硝酸溶液的PH约为2 |
| C.NaNO2溶液能使酚酞试液变红 |
| D.100mL l mol/L的亚硝酸溶液恰好与100mL l mol/L的NaOH溶液完全反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B.相同体积、相同浓度的盐酸与醋酸溶液,分别与同浓度的氢氧化钠溶液恰好完全反应时,醋酸消耗的氢氧化钠溶液体积多 |
| C.pH=11的NaOH溶液和pH=11的氨水分别稀释100倍后的pH前者一定小于后者 |
| D.分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 溶于水的电离方程式为___________________________。
溶于水的电离方程式为___________________________。 溶液中加入浓盐酸时,电离平衡向_________移动,
溶液中加入浓盐酸时,电离平衡向_________移动,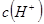 _________(填增大、减小、不变),
_________(填增大、减小、不变), _________(填增大、减小、不变)。
_________(填增大、减小、不变)。 溶液中加入
溶液中加入 固体,电离平衡向_________移动,
固体,电离平衡向_________移动,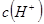 _________(填增大、减小、不变),
_________(填增大、减小、不变), _________(填增大、减小、不变)。
_________(填增大、减小、不变)。 溶液中
溶液中 增大,且使
增大,且使 的电离平衡逆向移动,可以加入_________。
的电离平衡逆向移动,可以加入_________。 溶液中加水,
溶液中加水, _________(填增大、减小、不变),溶液
_________(填增大、减小、不变),溶液 _________(填增大、减小、不变)
_________(填增大、减小、不变) 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②④⑤ | B.②④ | C.②③④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 在一定温度下,HCN在水中存在电离平衡:HCN
在一定温度下,HCN在水中存在电离平衡:HCN H+ + CN-。下列说法错误的
H+ + CN-。下列说法错误的 通入HCl气体,Q>K,平衡逆向移动
通入HCl气体,Q>K,平衡逆向移动 稀释溶液,电离平衡常数减小
稀释溶液,电离平衡常数减小 增大
增大查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是
CH3COO-+ H+ 的平衡体系中,加入下列物质能使醋酸的电离程度和溶液的pH都变大的是| A.NH4Cl固体 | B.CH3COONa | C.NH3·H2O | D.Zn粉 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com