
| A、5ab g | ||
| B、(a-5b)g | ||
C、(a-
| ||
D、
|
| bg |
| 32g/mol |
| b |
| 32 |
| ||
| 2(3-2) |
| b |
| 32 |
| b |
| 32 |
| b |
| 32 |
| b |
| 32 |
| 11 |
| 4 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | ||
| Z | W |
| A、常压下,W的常见单质有金刚石和石墨 |
| B、Z的阳离子与Y的阴离子电子层结构相同 |
| C、X的气态氢化物比Y的气态氢化物稳定 |
| D、W元素的金属性比Z元素的金属性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.
太阳能电池的发展已经进入了第三代.第一代为单晶硅太阳能电池,第二代为多晶硅、非晶硅等太阳能电池,第三代就是铜铟镓硒CIGS(CIS中掺入Ga)等化合物薄膜太阳能电池以及薄膜Si系太阳能电池.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KClO3和SO3溶于水能导电,故KClO3和SO3为电解质 |
| B、在蒸馏水中滴加浓H2SO4,Kw增大 |
| C、常温下将pH=4的醋酸溶液稀释后,溶液中导电离子的数目减少 |
| D、NaCl溶液和CH3COONH4溶液均呈中性,两溶液中水的电离程度相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、I- |
| B、SO42- |
| C、SO32- |
| D、NH4+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
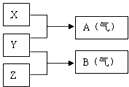 X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:
X、Y、Z为三种不同短周期非金属元素的单质.在一定条件下发生如下反应:若常温下Y为固体,X、Z为气体,A在空气中充分燃烧可生成B,则:查看答案和解析>>
科目:高中化学 来源: 题型:
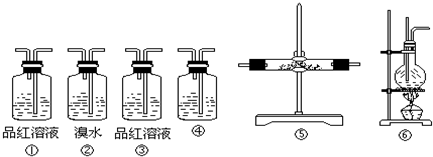
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com