
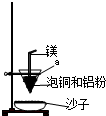
 工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.
工业上冶炼冰铜(mCu2O?nFeS)可得到粗铜,再以粗铜为原料制备硫酸铜晶体.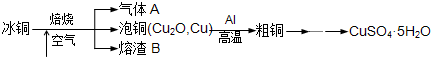
 ?CuY2-+2H+.则CuSO4?5H2O质量分数的表达式是______.
?CuY2-+2H+.则CuSO4?5H2O质量分数的表达式是______. 6Cu+Al2O3,
6Cu+Al2O3, 6Cu+Al2O3;
6Cu+Al2O3; =5bc×10-3mol,
=5bc×10-3mol,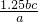 =
=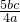 ,
,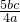 ;
;

科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验内容 | 实验现象 |
| A | 取第一份溶液,向其中滴加几滴酚酞试液,反复振荡. | 溶液不变红色 |
| B | 取第二份溶液,先加水稀释,再加少量的二氧化锰,有气泡放出,反复振荡,过滤,向滤液中滴加几滴酚酞试液,反复振荡. | 溶液变红色 |
| C | 取第三份溶液,向其中先加少量的二氧化锰,有气泡放出,反复振荡,过滤,向滤液中滴加几滴酚酞试液,反复振荡. | 溶液也不变红色 |
| D | 取第四份溶液,先加水稀释,再滴加几滴酚酞试液,反复振荡. | 溶液也不变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性强弱的顺序为Cl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com