
【题目】下列各组离子因发生氧化还原反应而不能大量共存的是( )
A.H+、Fe2+、NO3﹣、SO42﹣
B.Al3+、Na+、SO42﹣、HCO3﹣
C.Na+、Ca2+、Cl﹣、SO42﹣
D.Fe3+、K+、SCN﹣、Cl﹣
科目:高中化学 来源: 题型:
【题目】本题为《化学与生活(选修1)》选做题。
(1)资源必须要合理使用。
①水是一种宝贵的资源,保护水资源就是保护我们的生命。下列做法不利于水资源保护的是______(填字母代号)
A.科学合理使用农药 B.任意排放化工厂废水 C.处理生活污水,达标排放
②矿泉水瓶不能随意丢弃.根据垃圾分类方法,矿泉水瓶属于_____________(填“可回收物”或“可堆肥垃圾”);
③在汽车尾气系统中安装催化转化器,可有效降低尾气中CO和NO等向大气的排放,减小环境污染。在催化转化器中,CO和NO发生反应.请完成该反应的化学主程式_____________。
(2)保护环境、爱护地球已成为人们的共同呼声。
①我们常在公共场所见到下列标志,其中属于回收标志的是__________
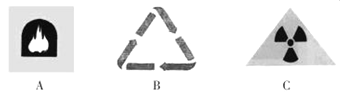
②2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中,不正确的是____________。
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、CO2、CO尼古丁和都属于室内空气污染物
(3)化学与生活关系密切。现有下列四种物质:
A.蛋白质 B.亚硝酸盐 C.维生素C D.油脂
①__________是重要的体内能源;
②__________广泛存在于新鲜水果和绿色蔬菜中,有酸性和还原性,又称为抗坏血酸;
(4)材料是人类赖以生存和发展的重要物质基础
①试管、烧杯和烧瓶等化学仪器的主要材质是__________;
A.玻璃 B.陶瓷 C.水泥
②“辽宁号”航母的服役举世瞩目。钢铁是制造航母的主要材料。生铁和钢成分上的主要差别是_________;
A.碳的含量不同
B.磷、硫的含量不同
C.镍、铬等金属含量不同
③钢铁在潮湿空气中易发生吸氧腐蚀,负极反应式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律正确的是
A. C、N、O最高正价依次升高
B. 钠、镁、铝的还原性依次减弱
C. HC1、HBr、HI的稳定性依次增强
D. H3PO4、H2SO4、HC1O的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为:HO-CH2-CH2-COOH,它是一种重要的有机化工原料,在一定条件下有如下转化(有的无机产物已省略)。
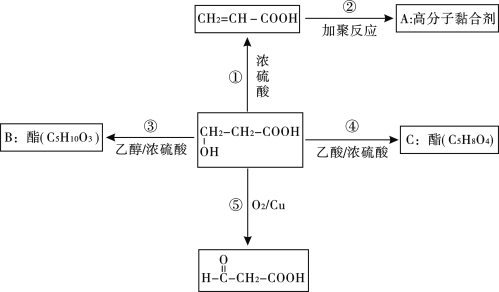
请回答:
(1)C的结构简式为________________。
(2)反应②、⑤的化学方程式为:②_________________________,⑤_________________________
③的反应类型______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
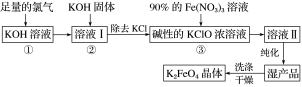
请回答下列问题:
(1)写出向KOH溶液中通入足量Cl2发生反应的离子方程式:________________________。
(2)在溶液Ⅰ中加入KOH固体的目的是____________(填字母)。
A.为下一步反应提供碱性的环境
B.使KClO3转化为KClO
C.与溶液Ⅰ中过量的Cl2继续反应,生成更多的KClO
D.KOH固体溶解时会放出较多的热量,有利于提高反应速率
(3)从溶液Ⅱ中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________________________________________________。每制得59.4 g K2FeO4,理论上消耗氧化剂的物质的量为________ mol。
(4)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,配平该反应的离子方程式:______ FeO42-+______ H2O===______ Fe(OH)3(胶体)+______ O2↑+______ OH-。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
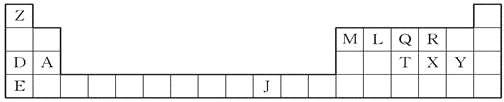
(1)T、X、Y原子的第一电离能由小到大的顺序是____________(用元素符号表示)。
(2)LX2分子的电子式是________________,XY2分子是____________(填“极性分子”或“非极性分子”);QY3分子中Q采用________杂化。
(3)由J、L、R三种元素形成的某种配位化合物,该化合物具有挥发性,化学式J(LR)4,其中J的化合价是0价。则基态J原子的核外电子排布式是___________________________;写出与配位体微粒互为等电子体的离子、分子各一种________、________。
(4)由Z、L、Q三种元素组成的化合物,分子式为Z9L3Q,它有_________种同分异构体(其中Q以三个单键与其他原子相连),请写出其中沸点最低的物质的结构简式__________________。
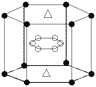
(5)A与M组成的一种化合物AM2,刷新了金属化合物超导温度的最高纪录。右图所示的是该化合物的晶体结构单元。图中上下底面中心“△”处的原子是________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
元素 | 有关性质或结构信息 |
A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
B | B原子得到一个电子后3p轨道全充满 |
C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物水化物的酸性为同主族最强 |
E | E元素的核电荷数等于A原子的核电荷数和B元素氢化物的核电荷数之和 |
(1)元素Y是C下一周期同主族元素,比较B、Y元素的第一电离能I1(B) I1(Y)(填“>”“=”或“<”);
(2)盐X的水溶液呈 (填“酸性”“碱性”或“中性”) ,原因________________(用离子方程式表示);
(3)E元素原子的核外电子排布式为_____________,在周期表中的位置______________;
(4)C单质分子中σ键和π键的个数比为 ,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是____________________________________________;
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式: ,写出该阳离子与硫的氢化物的水溶液反应的离子方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。已知:p(Ba2+)=-lgc(Ba2+),p(SO42-)=-lgc(SO42-).下列说法正确的是
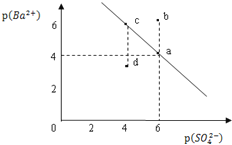
A. 该温度下,Ksp(BaSO4)=1.0×10-24
B. a点的Ksp(BaSO4)小于b点的Ksp(BaSO4)
C. d点表示的是该温度下BaSO4的不饱和溶液
D. 加入BaCl2可以使溶液由c点变到a点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2和NOx都是大气污染物。
(1)汽车排放的尾气中含CO和NO,汽车发动机工作时产生的NO和CO可通过催化转化器转化为两种无污染的气体,该反应的化学方程式是_________________________________________;
(2)采取还原法,用炭粉可将氮氧化物还原.
已知:N2(g)+O2(g)=2NO(g)△H=+180.6kJmol-1
C(s)+O2(g)=CO2(g)△H=-393.5kJmol-1
则反应C(s)+2NO(g)=CO2(g)+N2(g)△H=__________kJmol-1.
(3)将NO2变成无害的N2要找到适合的物质G与适当的反应条件,G应为_____________(填写“氧化剂”
或“还原剂”).下式中X必须为无污染的物质,系数n可以为0;
NO2+G![]() N2+H2O+nX (未配平的反应式);
N2+H2O+nX (未配平的反应式);
下列化合物中,满足上述反应式中的G是________(填写字母);
a.NH3 b.CO2 c.SO2 d.CH3CH2OH
(4)利用氨水可以将SO2和NO2吸收,原理如图1所示:NO2被吸收的离子方程式是______________;
(5)利用图2所示装置(电极均为惰性电极)也可吸收SO2,并用阴极排出的溶液吸收NO2.
①b极的电极反应式为__________________________;
②在碱性条件下,用阴极排出的溶液吸收NO2,使其转化为无害气体,同时有SO32-生成.该反应离子方程式为__________________________。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com