
下列物质中各含有少量杂质,能用饱和Na2CO3溶液并借助于分液漏斗除去杂质的是( )
A.苯中含有少量甲苯 B.乙醇中含少量乙酸
C.乙酸乙酯中含有少量乙酸 D.溴苯中含有少量苯
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案科目:高中化学 来源:2013-2014河北省高一下学期第三次月考化学试卷(解析版) 题型:选择题
将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )
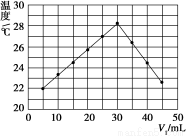
A.做该实验时环境温度为22 ℃
B.该实验可分多次把NaOH溶液倒入盛有盐酸的小烧杯中
C.NaOH溶液的浓度约为1.50 mol·L-1
D.该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市、定兴三中高二下学期期末化学试卷(解析版) 题型:填空题
(1)下列各组中的两种有机物,可能是相同的物质、同系物或同分异构体等,请判断它们之间的关系
①2-甲基丁烷和丁烷 。
②1-已烯和环已烷 。
(2)支链只有一个乙基且式量最小的烷烃的结构简式 。
(3)写出乙醛溶液与足量的银氨溶液共热的化学方程式: ;
(4)写出1,3-丁二烯与溴单质发生1,4-加成的反应方程式
(5)写出由乙醇一步制溴乙烷的化学方程式
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市、定兴三中高二下学期期末化学试卷(解析版) 题型:选择题
下列物质的俗称、主要成分及主要用途对应不正确的是
俗称 | 醋酸 | 石炭酸 | 福尔马林 | 四氯化碳 |
成分 | CH3COOH |
| HCHO | CCl4 |
用途 | 调味剂 | 环境消毒 | 防腐剂 | 灭火 |
选项 | A | B | C | D |
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市第二学期期中考试高二化学试卷(解析版) 题型:简答题
(10分)溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。某同学依据溴乙烷的性质,用右图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究。 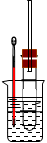
实验操作Ⅰ:在试管中加入5 mL 1 mol/L NaOH溶液和5 mL 溴乙烷,振荡。
实验操作II:将试管如图固定后,水浴加 热。
热。
(1)用水浴加热而不直接用酒精灯加热的原因是_______________________。
(2)观察到__ _______________________现象时,表明溴乙烷与NaOH溶液已完全反应。
_______________________现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是_______ ____。
(4)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是____________,检验的方法是 (需说明:所用的试剂、简单的实验操作及预测产生的实验现象)。
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市第二学期期中考试高二化学试卷(解析版) 题型:选择题
醇C5H11OH被氧化后可生成酮,该醇脱水时仅能得到一种烯烃,则这种醇是( )
A.C(CH3)3CH2OH B.CH(CH3)2CHOHCH3
C.CH3CH2CHOHCH3 D.CH3CH2CHOHCH2CH3
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市第二学期期中考试高二化学试卷(解析版) 题型:选择题
分子中含有5个碳原子的饱和一元醇,发生氧化后能生 成醛的种数与发生消去反应后生成烯烃的种数分别为 :( )
成醛的种数与发生消去反应后生成烯烃的种数分别为 :( )
A.5、6 B.4、5 C.4、6 D.5、5
查看答案和解析>>
科目:高中化学 来源:2013-2014河北省保定市第二学期期中考试高一化学试卷(解析版) 题型:简答题
(14分)从能量的变化和反应的快慢等 角度研究反应:
角度研究反应: 。
。
 (1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
(1)为了加快正反应速率,可以采取的措施有________(填序号,下同)。
A. 使用催化剂 B. 提高氧气的浓度
C. 提高反应的温度 D. 降低反应的温度
(2)已知该反应为放热反应,下图能正确表示该反应中能量变化的是______ __。
__。

(3)从断键和成键的角度分析上述反应中能量的变化。已知:化学键的键能:
化学键 | H—H | O=O | H—O |
键能 | 436 | 496 | 463 |
由此计算2molH2在氧气中燃烧生成气态水放出的热量
(4)已知1克氢气完全燃烧生成液态水放出QKJ的热量,则氢气燃烧生成液态水的热化学反应方程式为
(5)氢氧燃料电池的总反应方程式为 。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
。其中,氢气在________(填“正”或“负”)极发生________反应(填“氧化”或“还原”)。电路中每转移0.2mol电子,标准状况下消耗H2的体积是________L。
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省鹰潭市下学期期末质量检测高二化学试卷(解析版) 题型:实验题
(12分)某研究小组欲探究SO2的化学性质,设计了如下实验方案。
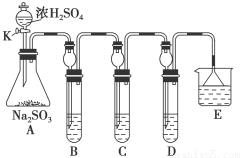
(1)在B中检验SO2的氧化性,则B中所盛试剂可为________。
(2)在C中装FeCl3溶液,检验SO2的还原性,则C中反应的离子方程式为__________________________。
(3)在D中装新制漂白粉浓溶液。通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分进行了探究。请回答下列问题:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1盐酸、0.5 mol·L-1H2SO4溶液、0.5 mol·L-1BaCl2溶液、品红溶液、新制澄清石灰水。
(ⅰ)假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为________;
假设三:该白色沉淀为上述两种物质的混合物。
(ⅱ)基于假设一,填写下表:
实验操作 | 预期现象和结论 |
将D中沉淀过滤,洗涤干净备用 |
|
用另一干净试管取少量沉淀样品,加入 ______ | __________ |
(ⅲ)若假设二成立,试写出生成该白色沉淀的化学方程式:
__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com