
| A、硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag |
| B、金属钠投入水中发生反应:2Na+2H2O=2Na++2OH-+H2↑ |
| C、向澄清石灰水中通入足量二氧化碳:OH-+CO2=HCO3- |
| D、碳酸钙溶于醋酸中:CaCO3+2H+=Ca2++2H2O+CO2↑ |


科目:高中化学 来源: 题型:
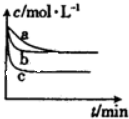 1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:
1000℃时,硫酸钠可与氢气发生反应:Na2SO4(s)+4H2(g)?Na2S(s)+4H2O(g).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
 将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,在图框中画出原电池的装置图,标出正、负极,并写出电极反应式.
将反应Cu+2FeCl3=CuCl2+2FeCl2设计成原电池,在图框中画出原电池的装置图,标出正、负极,并写出电极反应式.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
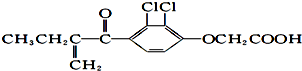
| A、利尿酸的化学式为:C13H14O4Cl2 |
| B、1mol 利尿酸最多可与4 mol H2发生反应 |
| C、利尿酸可使溴的四氯化碳溶液褪色 |
| D、利尿酸在一定条件下能发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.05mol/(L?s) |
| B、0.05mol/L |
| C、0.033 mol/(L?s) |
| D、0.075 mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、C(石墨)=C(金刚石),在该反应进程中其能量变化如下图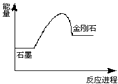 |
| B、Ba(OH)2?8H2O与NH4Cl反应 |
| C、灼热的碳与CO2反应 |
| D、甲烷在氧气中燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①② | B、② | C、①③ | D、②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v1 与v2同时增大 |
| B、v1 与v2同时减小 |
| C、v1增大,v2减小 |
| D、v1减小,v2增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com