
���淴Ӧ:2NO2(g) 2NO(g)+O2(g)���ܱ������з�Ӧ,�ﵽƽ��״̬�ı�־�� ( )
2NO(g)+O2(g)���ܱ������з�Ӧ,�ﵽƽ��״̬�ı�־�� ( )
�ٵ�λʱ��������nmolO2��ͬʱ����2nmolNO2
�ڵ�λʱ��������nmolO2��ͬʱ����2nmolNO
�۷ֱ���NO2��NO��O2�����ʵ���Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ2:2:1��״̬
�ܻ��������ɫ���ٸı��״̬�ݻ�������ܶȲ��ٸı��״̬
���������Է����������ٸı��״̬
A���٢ܢ� B���ڢۢ� C���٢ۢ� D���٢ڢۢܢݢ�

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
NAΪ�����ӵ����������������������
A����״���£�1molSO3(s)�����ԼΪ22.4L
B��100mL0.10 mol��L-1AlCl3��Һ�У�Cl-����ĿΪ0.03NA
C��18gˮ�У����ӵ���ĿΪ10NA
D��3molCu��ϡ������ȫ��Ӧ������ԭ��NO3-��ĿΪ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪�ֳ��������ѧУ�����ϵ�һ���ʼ컯ѧ�Ծ��������棩 ���ͣ��ƶ���
A��B��C��D��E�Ƕ�������ԭ�������������������Ԫ�أ�����Ԫ��A�ĵ����ڳ����³���̬��Ԫ��B��ԭ������������������Ӳ�����2����Ԫ��C��ͬ���ڵ�����Ԫ����ԭ�Ӱ뾶���Ԫ��D�ĺϽ����ճ������г��õĽ������ϡ����³�ѹ�£�E�����ǵ���ɫ���壬���ڻ�ɽ�ڸ���������
��1��CA��ˮ��Ӧ�ų�����Ļ�ѧ����ʽΪ ��
��2��B Ԫ�ص�Ԫ�ط��ţ� ��CA�ĵ���ʽΪ ��
D��Ԫ�����ڱ��е�λ��Ϊ ��
��3��A2E��ȼ���Ȧ�H �� ��a kJ��mol��1��д��A2Eȼ�շ�Ӧ���Ȼ�ѧ����ʽ�� ��
��4���ס��ҡ����ֱ���B��D��E����Ԫ����ۺ���������Σ��ס��Ҷ������������Ӧ���ұ�������ͬ����Ӧ�IJ��ﲻͬ���ش����⣺
�� �����Һ�л����μӹ���������Һ�����з�����Ӧ�����ӷ���ʽ �� ��
�� �����Һ�л����μӵ����ʵ����ı���Һ��������Һ������Ũ���ɴ�С��˳��Ϊ ��
��5����D������������ʯī��������NaHCO3��Һ�����Һ���е�⣬����������R��R���ȷֽ����ɻ�����Q��д����������R�ĵ缫��Ӧʽ�� ����R����Q�Ļ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʦ����ѧ������ѧ������һ��ģ������ѧ�Ծ��������棩 ���ͣ������
��14�֣���ҵ���������Ҫ��ӦΪ��4NH3 (g) +5O2 (g)  4NO(g) + 6H2O(l) ��H
4NO(g) + 6H2O(l) ��H
��1����֪������ȼ����Ϊ285.8kJ/mol��
N2��g��+3H2��g���T 2NH3��g����H = ��92.4kJ/mol��
N2��g��+ O2��g���T 2NO��g����H = +180.6kJ/mol��
��������ҵ���������Ҫ��Ӧ�ġ�H= ��
��2�����ݻ��̶����ܱ������з���������Ӧ�������ڲ������ʵ����ʵ���Ũ�����±���
Ũ�� | c(NH3)��mol/L�� | c(O2)��mol/L�� | c(NO)��mol/L�� |
��ʼ | 0.8 | 1.6 | 0 |
��2min | 0.6 | a | 0.2 |
��4min | 0.3 | 0.975 | 0.5 |
��6min | 0.3 | 0.975 | 0.5 |
��8min | 0.7 | 1.475 | 0.1 |
�ٷ�Ӧ�ڵ�2min����4minʱ��O2��ƽ����Ӧ����Ϊ ��
�ڷ�Ӧ�ڵ�6minʱ�ı����������ı������������ ������ţ���
A��ʹ�ô��� B�������¶� C����Сѹǿ D������O2��Ũ��
������˵������˵��4NH3(g) + 5O2(g)  4NO(g) + 6H2O(g)�ﵽƽ��״̬����_________ ������ţ���
4NO(g) + 6H2O(g)�ﵽƽ��״̬����_________ ������ţ���
A����λʱ��������n mol NO��ͬʱ������n mol NH3
B������һ������������ƽ����Է����������ٱ仯
C���ٷֺ���w��NH3��=w��NO��
D����Ӧ����v(NH3)��v(O2)��v(NO)��v(H2O) = 4��5��4��6
E�����ں��º�ѹ���ݻ��ɱ�������з�Ӧ�����������ܶȲ��ٱ仯
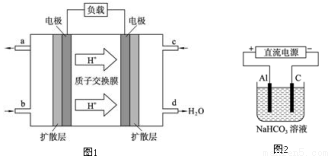
��3��ij�о�����װ��CH3OH��O2ȼ�ϵ�صĹ���ԭ����ͼ1��ʾ��
�ٸõ�ع���ʱ��b��ͨ�������Ϊ ��
�ڸõ�������ĵ缫��ӦʽΪ�� ��
���Դ˵������Դ����ʵ������ģ������Ʒ���桰�ۻ���������װ����ͼ2��ʾ���Ĺ����У�������Һ����Dz������ݲ�������ԭ������� ������ص����ӷ���ʽ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������������ѧ��һ��10�»�ѧ���������棩 ���ͣ�ѡ����
ʵ���������Ƹ�ˮ��Ӧ��ʵ��ʱ,�õ���������ҩƷ��:���ԹܼС������ӡ���С��������ֽ�����в������ձ�������������ʯ�������Უ��Ƭ����ҩ��.
A���٢ڢۢ� B���ڢۢܢޢ� C���ۢܢ��� D���ڢݢߢ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�츣��ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����д�����۾���������
ѡ�� | ���ӷ���ʽ | ���� |
A | ��2 mol Cl2ͨ�뵽��1 mol FeI2����Һ�У� 2Fe2����2I����2Cl2===2Fe3����4Cl����I2 | ��ȷ�� Cl2������Fe2����I���������� |
B | ��Cu�缫���NaCl��Һ�����ĵ缫��Ӧʽ�� 2Cl��-2e��===Cl2�� | ��ȷ�� Cl��������OH���ŵ� |
C | ����SO2ͨ�뵽NaClO��Һ�У� SO2��H2O��ClO��===HClO��HSO3- | ��ȷ�� H2SO3������ǿ��HClO |
D | Mg(HCO3)2��Һ��������NaOH��Һ��Ӧ�� Mg2����2HCO3-��4OH��=== Mg(OH)2 �� +2 CO32����2 H2O | ��ȷ�� Mg(OH)2��MgCO3������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ������
����β����ȼúβ������ɿ�����Ⱦ��ԭ��֮һ��

��1������β����������Ҫԭ��Ϊ2N0+2C0�� 2C02+N2�����ܱ������з����÷�Ӧʱ��c(C02)���¶ȣ�T)��ʱ�䣨t���ı仯������ͼ��ʾ��
��T1 (�>����������=��)T2
����T2�¶��£�0〜2 S�ڵ�ƽ����Ӧ���� ��N2)=��
��N2)=��
�����÷�Ӧ�ھ��ȡ����ݵ��ܱ���ϵ�н��У�����ʾ��ͼ��ȷ����˵����Ӧ�ڽ��е�t1ʱ�̴ﵽƽ��״̬���� ��

��2��NH3����ԭ��������(SCR)������ĿǰӦ�ù㷺���������������ѳ���������Fe������ʱ���ڰ�������������£���ͬ  ��Ӧ���ѵ�����ͼ��ʾ��
��Ӧ���ѵ�����ͼ��ʾ��

�ѵ�Ч����ѵ�= ����ʱ��Ӧ���ѵ���Ӧ�Ļ�ѧ����ʽΪ ��
��3��NO2��O2������NaNO3���γ�ȼ�ϵ�أ���ԭ����ͼ��ʾ���õ����ʹ�ù�����ʯīI�缫������N2O5,��缫��ӦʽΪ ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ��12���¿���ѧ�Ծ��������棩 ���ͣ��ƶ���
��֪������B��D��E��LΪ�ܶȱȿ���������壬D��EΪ���ʣ�����Ϊ�����A��һ�ֵ���ɫ���壬C����ˮ��F��G������L��ˮ��Һ��Ӧ�ų�B�����±߷�Ӧ��ͼ��ա�
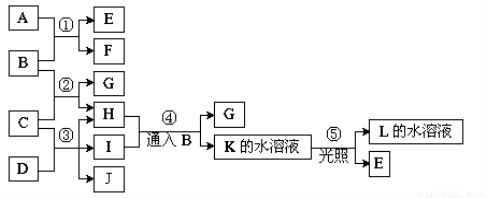
��1��F�������� ��B���ӵĽṹʽΪ____��ҵ�����÷�Ӧ������ ��
��2����Ӧ�ܵ����ӷ���ʽΪ ��
��3����һ�ֵ�������H��Ӧ����E���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��4��ij����M����Ư�����ã����������ԣ����л�ԭ�ԣ�Mͨ��D����Һ�з�
Ӧ�����ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ������ѧ�ڶ����ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У���Ϊ��Ӧ������Ũ�Ȼ�������ͬ��������ͬ��ѧ��Ӧ����
�� C��O2 �� Na��O2 ��Cu������ �� AlCl3��Һ��NaOH��Һ �� CO2��NaOH��Һ ��Fe��Cl2
A�������� B�����ۢ��� C�����ۢ��� D��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com