
| A、氯水中只含Cl2和H2O两种分子 |
| B、新制氯水只能使蓝色石蕊试纸变红 |
| C、光照氯水有气泡逸出,该气体是Cl2 |
| D、氯水放置数天后其pH将变小,酸性增强 |
| ||
| ||


 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、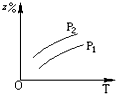 |
B、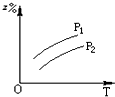 |
C、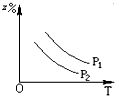 |
D、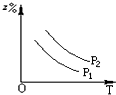 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、KNO3溶液 |
| B、K2CO3 溶液 |
| C、CuSO4 固体 |
| D、CH3COONa固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+ 1s22s22p63s23p6 |
| B、As 1s22s22p63s23p64s24p3 |
| C、N3- 1s22s22p6 |
| D、Cr 1s22s22p63s23p63d44s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、酸根离子中不可能含有金属元素 |
| B、铁比铝容易生锈,是因为铁比铝活泼 |
| C、向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+而没有Fe2+ |
| D、铝箔在酒精灯火焰山加热熔化但不滴落,因为铝箔表面的氧化铝熔点高于铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在电解池的阴极发生还原反应 |
| B、与电源负极相连的是电解池的阳极 |
| C、阴离子移向电解池的阳极 |
| D、电子从电源的负极沿导线流入电解池的阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、增大反应物浓度,活化分子百分数增大,化学反应速率增大 |
| B、难溶物质可能为强电解质,如BaSO4是强电解质 |
| C、放热反应的反应速率总是大于吸热反应的反应速率 |
| D、KW随浓度的改变而改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
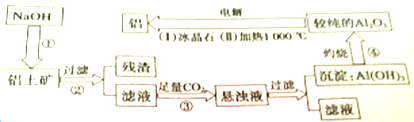
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com