
 X和1 mol Y,在一定条件下达到平衡,改变条件,其变化关系符合甲、乙图象。下列有关判断正确的是
X和1 mol Y,在一定条件下达到平衡,改变条件,其变化关系符合甲、乙图象。下列有关判断正确的是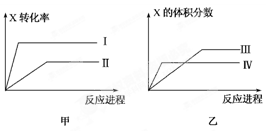
| A.甲图表示温度对X转化率的影响,且Ⅰ温度较低 |
| B.乙图一定表示压强对X体积分数的影响,且Ⅳ压强较高 |
| C.甲图一定表示压强对X体积分数的影响,且Ⅰ压强较高 |
| D.甲、乙图都可以表示温度、压强对平衡的影响,且Ⅰ>Ⅱ,Ⅲ<Ⅳ |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:填空题
 FeO(s)+CO(g)△H=akJ·mol—1,平衡常数为K;反应②CO(g)+1/2O2(g)=CO2(g) △H=bkJ·mol—1
FeO(s)+CO(g)△H=akJ·mol—1,平衡常数为K;反应②CO(g)+1/2O2(g)=CO2(g) △H=bkJ·mol—1| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
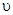 是速率、
是速率、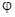 为混合物中CO含量,T为温度且T1>T2)
为混合物中CO含量,T为温度且T1>T2)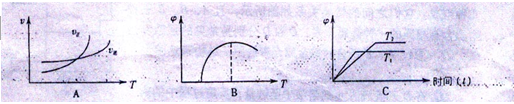
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 N2O4△H<0。现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。下列有说法正确的是
N2O4△H<0。现将一定量NO2和N2O4的混合气体通入一体积为1L的恒温密闭容器中,反应物浓度随时间变化关系如下图所示。下列有说法正确的是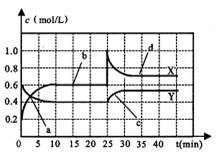
| A.曲线Y表示NO2浓度随时间的变化 |
| B.a点表示化学反应处于平衡状态 |
| C.c点表示v生成(NO2)< v消耗(NO2) |
| D.25min时,曲线发生变化的原因是缩小了容器的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2NH3(g) △H<0。使反应进行程度增大的方法是
2NH3(g) △H<0。使反应进行程度增大的方法是| A.升高温度 | B.降低压强 | C.使用催化剂 | D.及时分离出NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线
nQ(g)的平衡体系中,Q的物质的量浓度c(Q)与温度T的关系(曲线 上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是 ( )
上的任何一点都表示平衡状态)。下列有关该反应的描述错误的是 ( )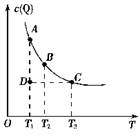
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
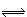 N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是
N2O4(正反应为放热反应)。将该烧瓶放在热水中,对现象的描述正确的是 | A.颜色不变 | B.颜色变浅 | C.颜色加深 | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3,并达到平衡,在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为:( )
2SO3,并达到平衡,在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率为:( )| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
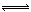 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 pC(g)+qD(g);△H<0 。下列结论中不正确的是
pC(g)+qD(g);△H<0 。下列结论中不正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com