
| A、c(H+)和c(OH-)的乘积 | ||||
B、
| ||||
C、
| ||||
| D、pH值 |
| c(OH -)C(NH 4 +) |
| c(NH 3?H 2O) |
| c(NH 3?H 2O) |
| C(OH -) |
| c(NH 4 +) |
| c(NH 3?H 2O) |


科目:高中化学 来源: 题型:
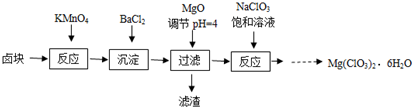
| A、卤块中加入KMnO4发生的氧化还原反应有2个 |
| B、加入BaCl2为沉淀SO42- |
| C、也可用Mg(OH)2代替MgO调节溶液的PH |
| D、在滤液中加NaClO3饱和溶液得到产品利用了相同温度下Mg(ClO3)2溶解度比NaClO3小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子p电子总数与s电子总数相等,且不与A元素在同一周期 |
| C原子所有轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
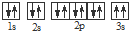 ,违背了
,违背了查看答案和解析>>
科目:高中化学 来源: 题型:
| |温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、33% | B、40% |
| C、50% | D、67% |
查看答案和解析>>
科目:高中化学 来源: 题型:
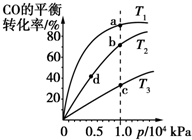 用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )
用CO合成甲醇(CH3OH)的化学反应方程式为CO(g)+2H2(g)?CH3OH(g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )| A、正反应速率:v(a)>v(c) v(b)>v(d) | ||||||||
| B、平衡时a点一定有n(CO):n(H2)=1:2 | ||||||||
| C、平衡常数:K(a)>K(c) K(b)=K(d) | ||||||||
D、平均摩尔质量:
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑥ | B、②③⑦ |
| C、①③⑥ | D、③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠具有很强的还原性 |
| B、钠原子的最外层只有一个电子 |
| C、在实验室中,钠通常保存在石蜡油或煤油中 |
| D、钠在常温下不易被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com