
| A、能源是有限的,无节制地利用常规能源,是一种盲目的短期行为 |
| B、根据能量守恒定律,担心能源枯竭是杞人忧天 |
| C、在能源的开发和利用中必须同时考虑对环境的影响 |
| D、人类的生存离不开能源,社会的进步和美好生活是以消耗大量能源为代价的,我们要珍惜能源 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

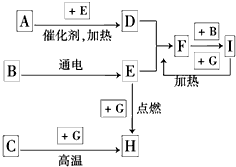
| A、X可能是一种氢化物 |
| B、M可能是金属 |
| C、E可能是一种有色气体 |
| D、F浓溶液能使某些金属钝化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、烯烃的加成反应、卤代烃和酯的水解反应、醛酮的还原反应都可引入羟基 |
| B、乙烯经过加成反应、消去反应可以得到乙炔 |
| C、取代反应、加成反应和消去反应都可引入卤素原子 |
| D、氧化反应、取代反应都可引入羧基 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钠可用于焙制糕点 |
| B、氨在常压冷却或常温加压的条件下可以液化为无色液体液氨,液氨的用途之一是用作生活中的制冷剂 |
| C、碳酸钡难溶于水和酸,可做X光透视胃的药剂 |
| D、每年春节全国各地齐放焰火充满新年气氛,这主要利用了化学中“焰色反应”的知识 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com