
A、 验证苯中是否有碳碳双键 |
B、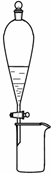 所示装置可分离CH3CH2OH和CCl4混合液 |
C、 所示装置可制取乙烯并验证其易被氧化 |
D、 所示装置可说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |


科目:高中化学 来源: 题型:
| ||
| t/min | 0 | 20 | 40 | 60 | 80 |
| c(H2O2)/mol?L-1 | 0.80 | 0.40 | 0.20 | 0.10 | 0.05 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaCl2 MgCl2 Na2O |
| B、H2O Na2O ? CO2 |
| C、CaCl2 ? NaOH H2SO4 |
| D、NH4Cl H2O CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | T | X | Y | Z |
| 性质 结构 信息 | 人体内含量最多的元素,且其单质是常见的助燃剂. | 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼. | 单质质软、银白色固体、导电性强. 单质在空气中燃烧发出黄色的火焰. | 第三周期元素的简单离子中半径最小 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、液体C为乙酸 |
| B、b溶液可以是硫酸 |
| C、操作I需用分液漏斗 |
| D、操作Ⅱ和操作Ⅲ都是蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、a>b+c |
| B、a=b+c |
| C、a<b+c |
| D、a=b=c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com