
【题目】铁片与稀硫酸反应制取氢气时,下列措施不能使氢气生成速率加大的是
A. 加热B. 滴加少量CuSO4溶液
C. 将铁片改用铁粉D. 增加稀硫酸的用量
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 煤的干馏就是加热除去煤中的水分,得到干燥的炭
B. 煤中含有甲苯、二甲苯等,可通过干馏得到
C. 以煤为主要原料,可以合成甲醇
D. 煤干馏得到的焦炉气不能与溴水反应而使溴水褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验以探究元素性质的递变规律,实验装置如图所示。
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3 , B装置中装有饱和碳酸氢钠溶液,C装置中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为 , C中可观察到的现象是。
(2)B装置的作用是。
(3)根据实验现象推知,碳酸、硝酸、硅酸的酸性强弱顺序是 , 由此得出碳、硅、氮三种元素非金属性的强弱顺序是。
(4)实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯和溴元素的非金属性强弱。
写出B装置中发生反应的离子方程式:。
(5)C装置的作用是。
(6)实验结论:氧化性 , 非金属性:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的( )
A. 在氧化还原反应中氧化剂表现氧化性
B. 在氧化还原反应中氧化剂被氧化
C. 复分解反应也可能是氧化还原反应
D. 没有单质参加的化合反应一定不是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用草酸的稀溶液或草酸钠的酸性溶液可以洗涤粘在皮肤上的高锰酸钾,其离子方程式为(未配平):MnO ![]() +C2O
+C2O ![]() +H+﹣→CO2↑+Mn2++.关于此反应的叙述正确的是( )
+H+﹣→CO2↑+Mn2++.关于此反应的叙述正确的是( )
A.该反应右边方框内的产物是OH﹣
B.配平该反应后,H+的化学计量数是8
C.该反应中氧化产物是CO2
D.该反应电子转移总数是5e﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质之间有如下转化关系: ![]()
(1)若甲是不溶于水的白色固体氧化物,既能溶于盐酸又能溶于氢氧化钠溶液,则甲是(填化学式);写出 乙→丙转化的离子方程式:。
(2)若乙溶液中加入KSCN溶液,有红色出现,则甲物质是(填化学式);写出 甲→乙转化的离子方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如右(部分反应中的水已略去). 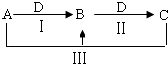
(1)若A为氯碱工业的产品,C为厨房中的用品.
①D的电子式是 .
②反应Ⅲ的离子方程式是 .
③氯碱工业制备A的化学方程式是 , 其中两种产物可与KI溶液反应制得一种化工原料,若消耗0.1mol KI转移电子0.6mol,则三种物质间反应的离子方程式是 .
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料.
①反应Ⅲ的离子方程式是 .
②B可作净水剂,在使用时发现B不能使酸性废水中的悬浮物沉降除去,其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是( )
选项 | a中物质 | b中物质 | c中收集气体 | d中物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | 浓盐酸 | HCl | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
A.A
B.B
C.C
D.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com