
将钠、镁、铝各0.3 mol分别放入足量的盐酸中,同温同压下产生的气体的体积比是( )
A.1∶1∶1 B.1∶2∶3 C.6∶3∶2 D.3∶1∶1
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
反应A+B→C(△H<0)分两步进行:①A+B→X(△H>0),②X→C(△H<0)。下列示意图中,能正确表示总反应过程中能量变化的是


A B C D
查看答案和解析>>
科目:高中化学 来源: 题型:
在甲、乙、丙、丁四个烧杯内分别放入0.1mol的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体完全溶解,则甲、乙、丙、丁所得溶液里溶质的质量分数大小顺序是 ( )
A.甲<乙<丙<丁 B.丁<甲<乙=丙
C.甲=丁<乙=丙 D.丁<甲<乙<丙
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两同学欲分别完成“钠与氯气反应”的实验.
I.甲同学的方案为:取一块绿豆大的金属钠(切去氧化层),用滤纸吸净煤油,放在石棉网上,用酒精灯微热.待钠熔成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方(装置如图I).该方案的不足之处有 钠预先在空气中加热,会生成氧化物,影响钠在氯气中燃烧;实验过程中会产生少量污染 (至少答出两点).
II.乙同学所采用的装置如图Ⅱ,回答下列问题:
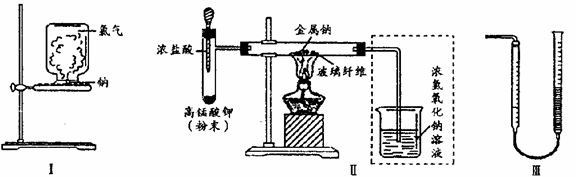
(1)按图Ⅱ组装仪器、添加药品,实验开始后,先将浓盐酸挤入试管,试管中发生反应的离子方程式为 2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O;待装置中出现 现象后,点燃酒精灯.
(2)点燃酒精灯后,玻璃管中出现的现象是 钠熔化并燃烧,产生黄色火焰,有白烟(至少答出两点)
(3)乙同学欲将虚框内装置改为图Ⅲ所示装置,并测量多余气体的体积.
①若图Ⅲ所示量气装置由干燥管、乳胶管和50mL滴定管组装而成,此处所用滴定管是
碱式(填“酸式”或“碱式”)滴定管.
②为提高测量的准确性,图Ⅲ装置中的液体可用 饱和NaCl溶液;收集完气体并冷却至室温后读数,读数前应进行的操作是 .
③如果开始读数时操作正确,最后读数时俯视右边滴定管液面,会导致所测气体的体积
(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目:高中化学 来源: 题型:
8g无水硫酸铜配成0.1 mol·L-1的水溶液,下列说法正确的是( )
A.溶于500mL水中 B.溶于1L水中
C.溶解后溶液的总体积为500mL D.溶解后溶液的总体积为1L
查看答案和解析>>
科目:高中化学 来源: 题型:
对相同质量的SO2和SO3 来说,下列关系正确的是 ( )
来说,下列关系正确的是 ( )
A.含氧原子个数比为2∶3 B.含氧元素质量比为5∶6
C.含硫原子个数比为5:4 D.含硫元素质量比为4∶5
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况下,CO和CO2的混合气体共67.2L,质量为116g.求:
(1)两种气体的物质的量之和为多少mol?
(2)其中CO2为多少 mol?
(3)CO的体积分数为多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 LH2(已折 算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
(1)甲的化学式是_________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________________________________-。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式_________。
有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之_________________________。
(已知Cu2O+2H+==Cu+Cu2++H2O)
(5)甲与乙之间_______(填“可能”或“不可能)发生反应产生H2,判断理由是____ ____。
____。
查看答案和解析>>
科目:高中化学 来源: 题型:
对相同状况下的12C18O和14N2两种气体,下列说法正确的是
 A.若质量相等,则质子数相等
A.若质量相等,则质子数相等
B.若原子数相等,则中子数相等
C.若分子数相等,则体积相等
D.若体积相等,则密度相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com