
 ȫ��������ϵ�д�
ȫ��������ϵ�д� һ��һ����ʱ���ϵ�д�
һ��һ����ʱ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 HCl+HClO��CaCO3����ˮ�е�HCl��Ӧ��ʹc��H+����С��ƽ�������ƶ���HClOŨ������Ư������ǿ
HCl+HClO��CaCO3����ˮ�е�HCl��Ӧ��ʹc��H+����С��ƽ�������ƶ���HClOŨ������Ư������ǿ HCl+HClO��CaCO3����ˮ�е�HCl��Ӧ��ʹc��H+����С��ƽ�������ƶ���HClOŨ������Ư������ǿ
HCl+HClO��CaCO3����ˮ�е�HCl��Ӧ��ʹc��H+����С��ƽ�������ƶ���HClOŨ������Ư������ǿ| ���� |
| �� |
| ���� |
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013-2014ѧ��ӱ�ʡ�����и�����һ��ģ�⿼�����ۻ�ѧ�Ծ��������棩 ���ͣ������
±��Ԫ�صĵ��ʺͻ�����ܶ࣬���ǿ���������ѧ���ʽṹ�����ʵ����֪ʶȥ��ʶ���������ǡ�
��1��±��Ԫ��λ�����ڱ���_______������ļ۵����Ų�ʽΪ____________________��
��2���ڲ�̫ϡ����Һ�У���������Զ����ӵ�(HF)2��ʽ���ڵġ�ʹ�������ӵϵ���������________________��
��3��������±��ṩ�ĵ�һ�����������жϣ����п������ɽ��ȶ��ĵ��������ӵ�±��ԭ����_________��
| �� | �� | �� | �� | �� |
��һ������ ��kJ/mol�� | 1681 | 1251 | 1140 | 1008 | 900 |
��4����֪�ߵ�����������ʽ����ѧʽ�ֱ�ΪH5IO6�� ����HIO4��ǰ��Ϊ��Ԫ�ᣬ����ΪһԪ�ᡣ��Ƚ϶�������ǿ����H5IO6_____HIO4������������������������������
����HIO4��ǰ��Ϊ��Ԫ�ᣬ����ΪһԪ�ᡣ��Ƚ϶�������ǿ����H5IO6_____HIO4������������������������������
��5������ˮ�е��ܽ����ȻС�����ڵ⻯����Һ���ܽ��ȴ������������������Һ�з������з�ӦI-+I2=I3-����KI3���Ƶģ�����CsICl2������֪CsICl2���ȶ��������ֽ⣬���������ɾ����ܸ�������ʣ�����������_____ʽ������
A��CsICl2=CsCl+ICl??????? B��CsICl2=CsI+Cl2
��6����֪ClO2-Ϊ���ͣ�������ԭ����Χ���ĶԼ۲���ӡ�ClO2-������ԭ�ӵ��ӻ��������Ϊ___________��д��һ��ClO2-�ĵȵ�����__________��
��7����֪CaF2���壨��ͼ�����ܶ�Ϊ�� g��cm-3��NAΪ�����ӵ�������������ڵ�����Ca2+�ĺ˼��Ϊa cm����CaF2����Է����������Ա�ʾΪ___________��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�����ʡ��������ƽ��ɽ������һ�ε��п��������ۺ����⣨��ѧ���֣� ���ͣ�ʵ����
��15�֣�
S2Cl2��һ���ӷ���Һ��(�۵㣺��76�棬�е㣺138��)��������ˮ����ˮ�ⷴӦ����������H2S��SO2��H2SO3��H2SO4�����ʡ����������������ڵ�����ͨ��������������S2Cl2����ͼ��ʵ������S��Cl2�Ʊ�S2Cl2��װ�� (�г�װ�á�����װ�þ�����ȥ)��
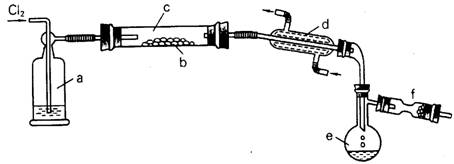
(1)��֪S2Cl2���ӽṹ��H2O2���ƣ���S2Cl2�ķ����й����� �����ۼ���
(2)װ��a��Ӧ���Լ�Ϊ ��װ��d�������� ������������ ��
(3)��ʵ��IJ���˳��ӦΪ (����ű�ʾ)��
�ټ���װ��c ��ͨ��Cl2 ��ͨ����ˮ ��ֹͣͨCl2 ��ֹͣ����װ��c
(4)ͼ��fװ����Ӧ���õ��Լ�Ϊ ��������Ϊ ��
(5)��S2Cl2��ˮ���������ͨ����ˮ�У����۲쵽 ���������֤��ˮ����������������ɡ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com