
【题目】NA是阿伏加德罗常数的值。下列说法正确的是
A. 常温下,11.2LSO2含有的氧原子数小于NA
B. 0. 1molNa2O2和Na2O的混合物中含有的离子总数等于0.4NA
C. 10g质量分数为34%的H2O2溶液含有的氢原子数为0.2NA
D. 100mL0.lmol/L醋酸中含有的醋酸分子数是0.0lNA
【答案】A
【解析】
A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L二氧化硫的物质的量小于0.5mol,则含有的氧原子个数小于NA,选项A正确;
B、由Na2O2的电子式为![]() ,Na2O的电子式为
,Na2O的电子式为![]() 可知,1 mol Na2O中含3mol离子,1molNa2O2中含3mol离子,则0. 1 mol Na2O和Na2O2混合物中离子为0.3mol,即含有的阴、阳离子总数是0.3NA ,选项B错误;
可知,1 mol Na2O中含3mol离子,1molNa2O2中含3mol离子,则0. 1 mol Na2O和Na2O2混合物中离子为0.3mol,即含有的阴、阳离子总数是0.3NA ,选项B错误;
C、H2O2溶液中,除了H2O2,水也含氢原子,故10g质量分数为34%的H2O2溶液中的氢原子的个数大于0.2NA个,选项C错误;
D. 醋酸为弱酸,在水中不完全电离,100mL0.lmol/L醋酸中含有的醋酸分子数小于0.0lNA,选项D错误。
答案选A。


 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:
【题目】关于 下列结论正确的是
下列结论正确的是
A. 该有机物分子式为C13H16
B. 该有机物属于苯的同系物
C. 该有机物分子至少有4个碳原子共直线
D. 该有机物分子最多有13个碳原子共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高能锂离子电池总反应式为2Li+FeS=Fe+Li2S,LiPF6·SO(CH3)2为电解质,用该电池为电源电解含镍酸性废水并得到单质Ni的实验装置如图所示。下列说法正确的是
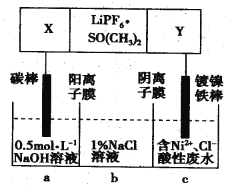
A. LiPF6·SO(CH3)2可用Li2SO4水溶液代替
B. 当转移1mol e-时,b室离子数增加NA个
C. 该电池充电时阳极反应式为Fe+Li2S-2e-=FeS+2Li+
D. 若去除图阴离子膜,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa。25℃时,H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1 mol·L-1 NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如图所示。下列说法不正确的是

A. a点溶液中:c(HA-)=c(H2A)
B. b点溶液中:A2-水解平衡常数Kh1=10-6.81
C. c点溶液中:V0=30
D. a、b、c、d四点中,d点溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】塑化剂(DEHP)的一种合成路线如下:

已知:①有机物分子中,同一个碳原子上连接两个羟基时不稳定,会自动脱水。
②
请回答下列问题:
(1)DEHP分子的官能团名称___________,B的名称___________。
(2)反应I、IV的类型分别为___________、___________;反应Ⅲ的条件___________。
(3)E的结构简式___________。
(4)反应V的化学方程式___________;
(5)符合下列条件的C的同分异构体共有___________种,写出其中一种的结构简式___________。
①遇FeCl3溶液显紫色 ②能发生银镜反应
③苯环上有三个取代基 ④能与 NaHCO3反应放出CO2气体
(6)请参考上述合成路线,以苯甲醇、正丁醇为原料,无机试剂任选,写出合成G(结构式如右)的路线流程图。合成路线流程图示例如下:
![]()

答:_______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列热化学方程式:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= —24.8 kJ·mol-1;3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ·mol-1 ;Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +19.4kJ·mol-1则14g CO气体与足量FeO充分反应得到Fe单质和CO2气体时的释放或吸收的热量为
A. 放出11 kJ B. 放出5.5kJ C. 吸收11 kJ D. 吸收5.5 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋植物如海带和海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋中提取碘的流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() ―→
―→![]()
某化学兴趣小组将上述流程②③设计成如下图所示操作。

已知过程②发生反应的化学方程式为Cl2+2KI===2KCl+I2
回答下列问题:
(1)写出提取过程①、③中实验操作的名称:①_____________ ③_____________
(2)四氯化碳是________色、密度比水________的液体。F中下层液体的颜色为________色,上层液体中溶质的主要成分为________。(填化学式)
(3)从F中得到固态碘还需进行的操作是___________________________。
(4)在灼烧过程中,使用到的实验仪器有(除泥三角外)_______________(填序号)。
①试管 ②瓷坩埚 ③坩埚钳 ④蒸发皿 ⑤酒精灯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,分别向NaA溶液和MCl溶液中加入盐酸和NaOH溶液,混合溶液的pH与离子浓度变化关系如下图所示。下列说法不正确的是

A. 曲线L1表示![]() 与pH的变化关系
与pH的变化关系
B. Ka(HA)=1×10-5.5
C. a点时两溶液中水的电离程度相同
D. 0.01mol·L-1MA溶液中存在:c(M+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学为探究H2O2、H2SO3、Br2氧化性强弱,设计如下实验(夹持仪器已略去,装置的气密性已检验)。

实验记录如下:

请回答下列问题:
(1)A中反应的离子方程式是__________________________________________________。
(2)实验操作Ⅱ吹入热空气的目的是_________________________________________。
(3)装置C的作用是____________,C中盛放的药品是_____________。
(4)实验操作Ⅲ,混合液逐渐变成红棕色,其对应的离子方程式_______________________。
(5)由上述实验得出的结论是_________________________________________________。
(6)实验反思:
①有同学认为实验操作Ⅱ吹入的热空气,会干扰(5)中结论的得出,你认为是否干扰,理由是_____________________________________________________________________。
②实验操作Ⅲ,开始时颜色无明显变化的原因是(写出一条即可):____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com