
| A. | 将AlCl3溶液和Al2(SO4)3溶液分别加热、蒸干、灼烧,所得固体成分相同 | |
| B. | 配制FeSO4溶液时,将FeSO4固体溶于稀盐酸中,然后稀释至所需浓度 | |
| C. | 用分液的方法分离乙醇和水的混合溶液 | |
| D. | 洗涤油污常用热的Na2CO3溶液 |
分析 A.氯化铝水解生成氢氧化铝和氯化氢,加热促进氯化氢挥发,从而促进氯化铝水解,将溶液蒸干得到氢氧化铝固体,硫酸铝水解生成氢氧化铝和硫酸,当溶液蒸干时,得到的固体是硫酸铝;
B.配制FeCl3溶液时,将FeCl3固体溶解在盐酸中抑制铁离子水解,硫酸溶液中引入硫酸根离子;
C.互不相溶的液体采用分液方法分离,互溶的液体采用蒸馏方法分离;
D.碳酸钠溶液中碳酸根离子水解其水溶液显碱性.
解答 解:A.氯化铝水解生成氢氧化铝和氯化氢,加热促进氯化氢挥发,从而促进氯化铝水解,将溶液蒸干得到氢氧化铝固体,硫酸铝水解生成氢氧化铝和硫酸,加热促进硫酸铝水解,因为硫酸没有挥发性,所以得到的固体仍然是Al2(SO4)3,故A错误;
B.Fe3+易水解,水解生成H+,水解的离子方程式为Fe3++3H2O?Fe(OH)3+3H+,配制溶液时,将FeSO4固体溶于稀盐酸中抑制FeSO4水解,然后再用水稀释到所需的浓度,盐酸溶液中引入氯离子,故B错误;
C.互不相溶的液体采用分液方法分离,互溶的液体采用蒸馏方法分离,乙醇和水互溶,所以应该采用蒸馏方法分离,故C错误;
D.纯碱溶液水解显碱性,升温促进水解,油脂在碱性条件下能发生水解,故D正确;
故选D.
点评 本题考查了盐类水解、溶液配制、混合物分离等,掌握基础是解题关键,题目难度不大.


科目:高中化学 来源: 题型:解答题
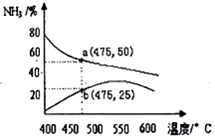 氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用.
氨是一种重要的化工原料,也是重要的工业产品,在工农业生产和国防等领域发挥着重要作用.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四个碳原子不可能在一条直线上 | B. | 所有原子在同一平面内 | ||
| C. | 在同一直线上的原子最多为4个 | D. | 在同一直线上的原子最多为6个 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 发生水合过程,并且放出热量 | |
| B. | 发生扩散过程,并且放出热量 | |
| C. | 水合过程放出的热量大于扩散过程吸收的热量 | |
| D. | 扩散过程放出的热量大于水合过程吸收的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ④ | C. | ①②④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 | |
| B. | 用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定 | |
| C. | 用碱式滴定管取10.00mLNaOH溶液放入用蒸馏水洗净的锥形瓶中进行滴定 | |
| D. | 用酚酞作指示剂滴至红色刚变无色时即停止加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
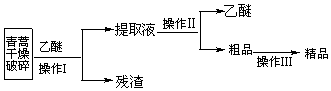
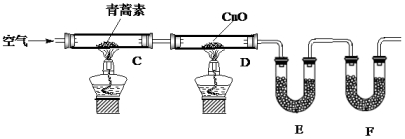
| 装置 | 实验前 | 实验后 |
| E | 24.00g | 33.90g |
| F | 100.00g | 133.00g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com