
【题目】下列说法错误的是
A.铅蓄电池是二次电池
B.碱性锌锰电池不是一次电池
C.一般化学电池的活性物质储存在电池内部,限制了电池容量
D.二次电池又叫蓄电池,它放电后可以再充电使活性物质获得再生
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】天然气是一种重要的清洁能源和化工原料,其主要成分为甲烷。
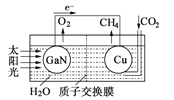
(1)科学家用氮化镓材料与铜组装如右图的人工光合系统, 利用该装置成功地实现了以CO2和H2O合成CH4。
①写出铜电极表面的电极反应式 。
②为提高该人工光合系统的工作效率,可向装置中加入少量 (选填“盐酸”或“硫酸”)。
(2)天然气中的H2S杂质常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式 。
(3)天然气的一个重要用途是制取H2,其原理为:CO2(g)+CH4(g) ![]() 2CO(g)+2H2(g) 。
2CO(g)+2H2(g) 。
①该反应的平衡常数表达式为 。
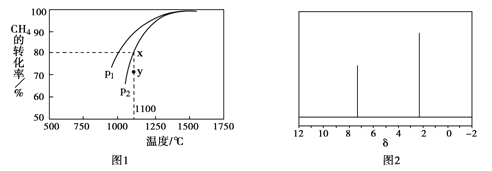
②在密闭容器中通入物质的量浓度均为0.1mol·L-1的CH4与CO2,在一定条件下发生反应,测得CH4的平衡转化率与温度及压强的关系如下图1所示,则压强P1 P2(填“>”或“<”);压强为P2时,在Y点:v(正) v(逆)(填“>”、“<”或“=”)。
(4)天然气也可重整生产化工原料,最近科学家们利用天然气无氧催化重整获得芳香烃X。由质谱分析得X的相对分子质量为106,其核磁共振氢谱如下图2,则X的结构简式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活、社会发展息息相关,下列说法不正确的是( )
A.“熬胆矾铁釜,久之亦化为铜”,该过程发生了置换反应
B.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
C.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着人们生活质量的不断提高,废电池必须进行集中处理的问题被提到议事日程,其首要原因是
A.回收其中的石墨电极
B.利用电池外壳的金属材料
C.防止电池中汞、镉和铅等重金属离子对土壤和水资源的污染
D.不使电池中渗泄的电解质腐蚀其他物品
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于判断过程的方向的说法正确的是
A.所有自发进行的化学反应都是放热反应
B.同一物质的固、液、气三种状态的熵值相同
C.石墨比金刚石稳定,故石墨转化为金刚石的反应可以自发进行
D.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行了如下实验。
【分子式的确定】
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6.72L(标准状况)。则该有机物中各元素的原子个数比是 。
(2)该有机化合物的相对分子质量为46,则其分子式是 。
(3)预测A的可能结构并写出结构简式 。
【结构简式的确定】
(4)经测定,在标准状况下0.2mol有机物A与足量金属钠反应生成2.24L的氢气,则A的结构简式为 。理由__________________。
【性质实验】
(5)A在一定条件下脱水可生成B,用B制备氯乙烷原子利用率为100%,请写出上述由B制备氯乙烷反应的化学方程式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活、环境等社会实际密切相关。下列叙述正确的是
A.“滴水石穿、绳锯木断”不涉及化学变化
B.明矾净水的原理和“84”消毒液消毒的原理不相同
C.氟利昂作制冷剂会加剧雾霾天气的形成
D.汽车尾气中含有的氮氧化物,是汽油不完全燃烧造成的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一氯甲烷(CH3C1)是一种重要的化工原料,常温下它是无色有毒气体,微溶于水,易溶于乙醇、CCl4等。
(1)甲组同学在实验室用下图所示装置模拟催化法制备和收集一氯甲烷。
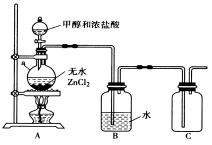
① 无水ZnCl2为催化剂,a瓶中发生反应的化学方程式为____________________________。
② 装置B的主要作用是____________________。
③收集到的CH3Cl气体在氧气中充分燃烧,产物用过量的V1mL、c1mol·L-1NaOH溶液充分吸收,以甲基橙作指示剂,用c2 mol·L-1盐酸标准液对吸收液进行返滴定(发生的反应为:
NaOH+HCl= NaCl+H2O ,Na2CO3+2HCl=2NaCl+2CO2↑+2H2O),最终消耗V2 mL盐酸。则所收集CH3Cl的物质的量为_____ _ mol。(已知:2CH3Cl+3O2![]() 2CO2+2H2O+2HCl)
2CO2+2H2O+2HCl)
(2)乙组同学选用甲组A、B装置和下图所示的部分装置检验CH3Cl中的氯元素。
(已知:一卤代烷一般要在加热条件下才能与氢氧化钠溶液反应)
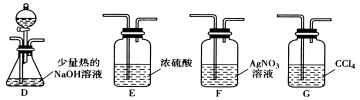
①乙组同学的实验装置中,依次连接的合理顺序为A→B→________→__ → 。
②通入一段时间的CH3Cl气体,打开装置D中分液漏斗的活塞,观察实验现象。分液漏斗中盛放的试剂是_______和_________。
③能证明CH3Cl中含有氯元素的实验现象是_____________________________。
(3)查阅资料可知:AgNO3的乙醇溶液可以检验CH3X中的卤素原子。相关数据如下表:

①CH3X通入AgNO3的乙醇溶液中,除有沉淀生成外,还生成硝酸甲酯,请写出硝酸甲酯的结构简式:______________________________。
②将CH3Cl和CH3Br的混合气体通入AgNO3的乙醇溶液中,先出现淡黄色沉淀。请依据表中数据解释原因____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com