
 四甲基氢氧化铵常用作计算机硅片面用光亮剂和触刻剂,工业上以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵 溶液的原理如图所示,下列说法不正确的是( )
四甲基氢氧化铵常用作计算机硅片面用光亮剂和触刻剂,工业上以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵 溶液的原理如图所示,下列说法不正确的是( )| A. | b极为阴极,发生还原反应 | |
| B. | a处产生的气体能使湿润的淀粉碘化钾试纸变蓝 | |
| C. | 外电路电子的流向为M→a,b→N | |
| D. | 电解反应的总化学方程式为2(CH3)4NCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2(CH3)4NOH+H2↑+Cl2↑ |
分析 工业上以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵,图中四甲基氢氧化铵在b电极生成,说明溶液中氢离子在b电极得到电子发生还原反应生成氢气,a为阳极,氯离子失电子发生氧化反应生成氯气,M为电源正极,N为电源负极,据此分析选项.
解答 解:工业上以石墨为电极电解四甲基氯化铵溶液制备四甲基氢氧化铵,图中四甲基氢氧化铵在b电极生成,说明溶液中氢离子在b电极得到电子发生还原反应生成氢气,a为阳极,氯离子失电子发生氧化反应生成氯气,M为电源正极,N为电源负极,
A.上述分析可知b极为阴极,发生还原反应,故A正确;
B.a为阳极,氯离子失电子发生氧化反应生成氯气,能使湿润的淀粉碘化钾试纸变蓝,故B正确;
C.外电路电子的流向是阳极到电源正极,电源负极到阴极,a→M,N→b,故C错误;
D.溶液中氢离子在b电极得到电子发生还原反应生成氢气,a为阳极,氯离子失电子发生氧化反应生成氯气,电解反应的总化学方程式为2(CH3)4NCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2(CH3)4NOH+H2↑+Cl2↑,故D正确;
故选C.
点评 本题考查了电解原理的分析、电解反应的电极判断、电极反应、电子流向、电解反应等知识点,掌握基础是解题关键,题目难度中等.


 全能练考卷系列答案
全能练考卷系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解法制铝时,一般用熔融态的氧化铝进行电解,但也可用其相应的盐,如熔融态的AlCl3 | |
| B. | 电解法生产铝时,需对铝土矿进行提纯,在提纯过程中应用了氧化铝或氢氧化铝的两性 | |
| C. | 在氯碱工业中,电解池中的阴极产生的是H2,NaOH在阳极附近产生 | |
| D. | 氯碱工业和金属钠的冶炼都用到了NaCl,在电解时它们的阴极都是Cl-失电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该盐的名称为硝酸铵 | B. | 该盐的水溶液pH<7 | ||
| C. | 该盐的化学式为NH4HCO3 | D. | 该盐可做氮肥,不宜与草木灰混用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是物质的质量的单位 | |
| B. | 碳的摩尔质量为12g | |
| C. | 阿伏加德罗常数约为6.02×1023mol-1 | |
| D. | 一个碳原子的质量为12g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
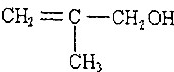
| A. | 只有① | B. | ①和② | C. | ①和④ | D. | ③和④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(HCO3)2与NaOH溶液反应 | B. | Mg(HCO3)2与NaOH溶液反应 | ||
| C. | Ca(HCO3)2与澄清石灰水反应 | D. | NH4HCO3与澄清石灰水反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
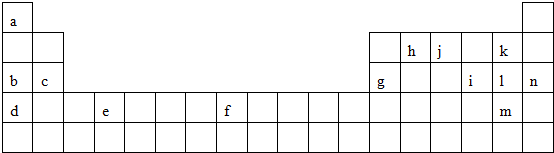

 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
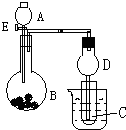 用如图所示装置进行实验,将A逐滴加入B中:
用如图所示装置进行实验,将A逐滴加入B中:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com