
某元素x的最高价含氧酸的化学式为HnXO2n-2:,则在其气态氢化物中,x元素的化合价为
A.一(12—5n) B.一(12—3n) C.一(6—3n) D.一(10一n)
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
已知: C(s)+H2O(g)=CO(g)+H2(g) ΔH=akJ·mol-1
C(s)+ 1/2 O2(g) =CO(g) ΔH=-110kJ·mol-1
H-H、O=O和O-H键的键能分别为436、496和462kJ·mol-1,则a为
A.-332 B.-118 C.+350 D.+130
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是
A.足量的CO2通入饱和碳酸钠溶液中CO2+CO32-+H2O=2HCO3-
B.FeSO4溶液在空气中变质:4Fe2++O2+2H2O=4Fe3++4OH-
C.向NaAlO2溶液中通入过量CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
D.碳酸氢镁溶液加入过量石灰水
Mg2++2HCO3-+2Ca2++4OH-=2CaCO3↓+Mg(OH)2↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是中学常见的5种化合物,A、B是氧化物,元素X、Y的单质是生活中常见的金属,相关物质间的关系如下图所示。
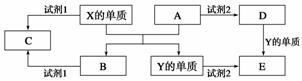
(1)X的单质与A反应的用途是________________▲_____________________。
(2)若试剂1是NaOH溶液,X的单质与试剂1反应的离子方程式是____ ▲__________
(3)若试剂1和试剂2均是稀硫酸:
①检验物质D的溶液中金属离子的试剂可以是________▲_______(填名称)
②将物质C溶于水,其溶液呈酸性,原因是(用离子方程式表示)______ ▲____________。
③某高效净水剂是由Y(OH)SO4聚合得到的。工业上以E、稀硫酸和亚硝酸钠为原料来制备Y(OH)SO4,反应中有NO生成,该反应的化学方程式是_________▲_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于元素周期表的说法正确的是
A.能生成碱的金属元素都在ⅠA族
B.原子序数为14的元素位于元素周期表的第3周期ⅣA族
C.稀有气体元素原子的最外层电子数均为8
D.第二周期ⅣA族元素的原子核电荷数和中子数一定为6
查看答案和解析>>
科目:高中化学 来源: 题型:
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子,在ag HmX中所含质子的物质的量是
A.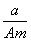 (A-N)mol B.
(A-N)mol B.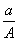 (A-N)mol C.
(A-N)mol C.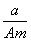 (A-N+m)mol D.
(A-N+m)mol D. 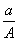 (A-N+m)mol
(A-N+m)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D四种元素,其原子序数大小关系为A>B>C>D。已知将0.5mol 某元素A原子的最高价离子还原成中性原子时,需得到6.02×1023个电子,当A的单质同盐酸充分反应放出0.02 g氢气时,用去0.4gA单质。A原子中质子数等于中子数。B元素原子的核外电子层数和A相同。C元素的氧化物既溶于强酸,也溶于强碱。D元素的氢化物为DH3。 试回答:
⑴ 元素符号: B C
⑵ C的单质与B的最高价氧化物的水化物溶液反应的化学方程式为
写出A与盐酸反应的离子方程式为
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A2(g)+2B2 (g) 2AB2 (g)的ΔH<0,下列说法正确的是( )
2AB2 (g)的ΔH<0,下列说法正确的是( )
A.升高温度,正向反应速率增加,逆向反应速率减小
B.升高温度有利于反应速率增加,从而缩短达到平衡的时间
C.达到平衡后,升高温度或增大压强都有利于该反应平衡正向移动
D.达到平衡后,降低温度或减小压强都有利于该反应平衡正向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质中既能跟稀硫酸反应,又能跟氢氧化钠溶液反应的是
①NaHCO3 ②(NH4)2SO3 ③Al2O3 ④Al(OH)3⑤Al
A. 全部 B.①③④⑤ C.②③④⑤ D.③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com