
【题目】(1)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、⑤C2H6、⑥CH3CH=CH2中,一定互为同系物的是_______,一定互为同分异构体的是________________(填编号);
(2)以五倍子为原料可制得A,A结构简式为下图所示,回答下列问题:
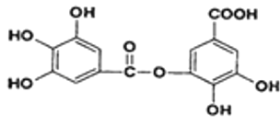
①A的分子式为______________;
②有机化合物B在硫酸催化条件下加热发生酯化可得到A。写出B的结构简式为_____ ;
(3)写出含有1个-CH2-、1个![]() 、3个-CH3原子团的烃类物质的结构简式___________;
、3个-CH3原子团的烃类物质的结构简式___________;
(4)写出核磁共振氢谱有两组峰,且峰面积之比为3:2,分子式为C8H10的芳香烃类化合物的结构简式_________;
(5)写出该有机物的名称![]() ________________。
________________。
【答案】②⑥ ③④ C14H10O9 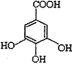
![]()
![]() 3-甲基-2-丁醇
3-甲基-2-丁醇
【解析】
(1)结构相似,在分子组成上相差一个或若干个CH2原子团的物质互称为同系物;分子式相同,结构不同的有机物互称为同分异构体,根据以上概念进行分析判断;
(2)①由结构简式可知分子中的原子个数,从而确定分子式;②利用逆推法可知,A水解生成B;
(3)甲基只能出现在碳链的端点,根据所给原子团书写;
(4)根据分子式计算碳的不饱和度,核磁共振氢谱有两组峰就是该有机物中有两种等效氢原子,峰面积之比就是等效氢原子个数之比;
(5)根据有机物的系统命名法进行命名。
(1)②CH2=CH2和⑥CH3CH=CH2结构相似,都属于烯烃,分子组成相差1个CH2原子团,互为同系物;③CH3CH2C≡CH和④CH3C≡CCH3分子式相同,结构不同,互为同分异构体,故答案为:②⑥;③④;
(2)①由A的结构简式可知分子式为C14H10O9;
②由有机化合物B在硫酸催化条件下加热发生酯化可得到A可知,A水解生成B,所以B为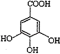 ,故答案为:C14H10O9;
,故答案为:C14H10O9;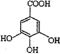 ;
;
(3)甲基只能出现在碳链的端点,一条碳链有两个端点也就是两个甲基,三个甲基就是再有一个甲基作为支链,所以含有1个-CH2-、1个![]() 、3个-CH3原子团的烃类物质的结构简式为:
、3个-CH3原子团的烃类物质的结构简式为:![]() ;
;
(4)分子式为C8H10的芳香烃类化合物中碳的不饱和度为8+1-![]() =4,苯环的不饱和度为4,故除了苯环之外再无不饱和键,核磁共振氢谱有两组峰说明该有机物只有2种等效氢原子,峰面积之比为3:2即2种等效氢原子的个数之比为3:2,综上可知该有机物为高度对称结构,苯环外的两个碳原子应该为处于对位的两个甲基,结构简式为:
=4,苯环的不饱和度为4,故除了苯环之外再无不饱和键,核磁共振氢谱有两组峰说明该有机物只有2种等效氢原子,峰面积之比为3:2即2种等效氢原子的个数之比为3:2,综上可知该有机物为高度对称结构,苯环外的两个碳原子应该为处于对位的两个甲基,结构简式为:![]() ;
;
(5)该有机物中有一个羟基官能团属于醇,从靠近羟基的一端开始编号,主链共有四个碳原子,2号碳上有一个羟基,3号碳上有一个甲基,该有机物命名为:3-甲基-2-丁醇。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某研究性学习小组对某废旧合金(含有Cu、Fe、Si 三种成分)进行分离、回收。其工业流程如图:
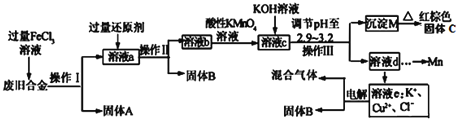
已知:298K时,Ksp[Cu(OH)2]=2.0×10-20,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Mn(OH)2]=1.9×10-13,根据上面流程回答有关问题:
(1)操作Ⅰ、Ⅱ、Ⅲ一定都不含有的操作是________
A.过滤 B.洗涤 C.干燥 D.蒸馏
(2)过量的还原剂应是________,溶液a中发生的反应的离子方程式为________;
(3)将溶液c调节pH至2.9~3.2的目的是________;
(4)常温下,取2mol/L的CuCl2溶液,若要使Cu2+开始沉淀,应调节pH至________;
(5)工业上由红棕色固体C制取相应单质常用的方法是________。
A.电解法 B.热还原法 C.热分解法
(6)用惰性电极电解溶液e制取固体B,阳极主要发生的电极反应为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为中学化学常见的单质或化合物,其中A、F为单质,常温下,E的浓溶液能使铁、铝钝化,相互转化关系如图所示(条件已略去)。完成下列问题:

(1)若A为淡黄色固体,B为气体,F为非金属单质。
①写出E转变为C的化学方程式________________________________。
②B在空气中能使银器表面失去金属光泽、逐渐变黑,该反应的氧化剂和还原剂之比为_____。
(2)若B为能使湿润的红色石蕊试纸变蓝的气体。
①B和E反应得到的产物中所含的化学键类型为____________________。
②做过银镜反应后的试管可用E的稀溶液清洗,反应的离子方程式为___________________。
③在干燥状态下,向②反应得到的溶质中通入干燥的氯气,得到N2O5和一种气体单质,写出反应的化学方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1cm滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上。关于图1图2中的实验有以下说法,其中正确的是( )
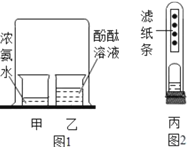
①图2比图1的实验减少了大气污染、更节约
②图1和图2的实验均能证明分子在不断运动
③图2中观察到的现象是滤纸条上的酚酞试液自上而下依次变红
④若另取与丙相同的装置浸入10℃的冷水中,则不能得出结论
A.①②B.①②④C.①②③④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁红(Fe2O3)是一种常见颜料,用废铁屑制取铁红的工艺如图:

(1)写出废铁屑中的铁和稀硫酸反应的离子方程式:_____。
(2)“沉淀”反应中除生成FeCO3外,还生成一种能使澄清石灰水变浑浊的气体,该气体为_____。
(3)检验滤液中含有![]() 的方法是_____。
的方法是_____。
(4)“煅烧”时FeCO3与O2反应的物质的量之比为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】漂白粉是常见的消毒剂,实验室可利用如图所示装置制取:
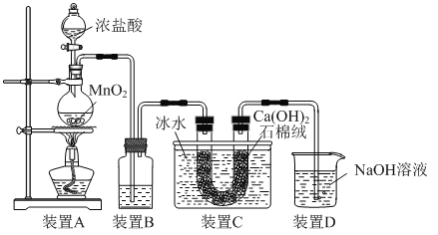
(1)装置A中所发生反应的化学方程式为_____。
(2)为除去挥发出的HCl,装置B中应装有_____。
(3)装置C中所发生反应的化学方程式为_____。
(4)装置D的作用是_____。
(5)有效氯含量是衡量次氯酸盐氧化能力的重要指标。次氯酸盐的有效氯含量可用次氯酸盐与盐酸反应所生成的氯气的含量表示:Cl—+ClO—+2H+=Cl2+H2O[有效氯含量=![]() ×100%]。为测定装置C中所得漂白粉的有效氯含量,进行如下实验:准确称取装置C中所得漂白粉1.775g,将其与浓盐酸反应,所得Cl2在标准状况下的体积为0.112L。计算漂白粉的有效氯含量,并写出计算过程_____。
×100%]。为测定装置C中所得漂白粉的有效氯含量,进行如下实验:准确称取装置C中所得漂白粉1.775g,将其与浓盐酸反应,所得Cl2在标准状况下的体积为0.112L。计算漂白粉的有效氯含量,并写出计算过程_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时拟用0.10mol/L的氢氧化钠溶液滴定10mL浓度为0.10mol/L醋酸的滴定曲线如图所示。横坐标为加入氢氧化钠的体积,纵坐标为溶液的pH。回答下列问题:
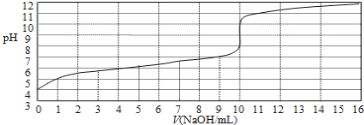
(1)该醋酸溶液的电离度α=______________。
(2)写出pH=7时溶液中离子浓度的大小关系:__________________________ 。
(3)为了准确指示终点本次滴定最好选用________做指示剂。
(4)写出滴入5mL氢氧化钠溶液时,溶液中的物料守恒关系:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数的值,下列说法中正确的是( )
①1mol Na2O 和 Na2O2 混合物中含有的阴、阳离子总数是 3NA
②常温常压下,92g的NO2和N2O4 混合气体含有的原子数为 6NA
③7.8 g![]() 中含有的碳碳双键数目为 0.3 NA
中含有的碳碳双键数目为 0.3 NA
④用 1L1.0 mol/LFeCl3 溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为 NA
⑤1mol SO2与足量O2在一定条件下充分反应生成 SO3,共转移 2NA个电子
⑥在反应 KIO3+6HI=KI+3I2+3H2O 中,每生成 3molI2 转移的电子数为 5NA
A.①②③B.②③④C.①②⑥D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计用如图所示实验装置(夹持仪器省略)制取干燥的氨气并验证NH3具有还原性,请回答下列问题:
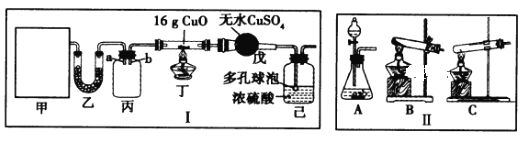
(1)实验室制备氨气有多种方法,现欲用NH4C1与Ca(OH)2反应制取NH3,则甲中的气体发生装置___________(从Ⅱ中选用);用浓氨水与生石灰反应也可制取NH3,反应的化学方程式为__________
(2)装置丙用于收集NH3,应将导管__________(填“a”或“b”)延长至集气瓶底部,装置乙中盛放的试剂为__________,装置己的作用为____________(答两点)。
(3)若装置丁中黑色固体变红,则装置戊中现象为_________
(4)研究小组的同学通过讨论、分析后认为充分反应后生成的红色固体可能是Cu或Cu2O或二者的混合物,通过查阅资料知:Cu2O+2H+=Cu+Cu2++H2O。为探究固体的成分,提出了如下两种方案。
I. 甲同学取少量红色固体与稀硝酸混合,最终得到蓝色溶液,由此推测红色产物中有Cu2O。
①你对甲同学实验设计的评价是__________(请给出必要的文字解释)。
②Cu2O与稀硝酸反应的离子方程式为_____________
Ⅱ.乙同学认为不需要借助任何化学试剂,只需要称量生成的红色固体的质量(设为xg)就能确定产物成分,当x取值范围为 _____时,表明产物中既有Cu,又有Cu2O。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com