
| A�� | ԭ�Ӱ뾶��Y��Z��R��T | |
| B�� | XR2��WR2����������R�Ļ��ϼ���ͬ | |
| C�� | ��̬�⻯����ȶ��ԣ�W��R��T | |
| D�� | ����������Ӧ��ˮ������ԣ�X��Z |
���� ����ʯ��è����ǰ20��Ԫ���е�6����ɣ��仯ѧʽΪX3Y2��ZWR4��3T2������Rԭ������������Ϊ�������������3����Rԭ��ֻ����2�����Ӳ㣬����������Ϊ6����RΪOԪ�أ�Y��Z��R��Tλ��ͬ���ڣ������ڵڶ����ڣ�TԪ�������ۣ���TΪFԪ�أ�Z�������������������������ȣ���ZΪBeԪ�أ�YΪ����Ԫ�أ���YΪLi��X��Zλ��ͬ���壬��XΪMgԪ�ػ�CaԪ�أ���XΪþԪ�أ�����X��Rԭ������֮����W��2������$\frac{12+8}{2}$=10���Ƴ�WΪ��Ԫ�ز��������⣬��XΪCaԪ�أ�����X��Rԭ������֮����W��2������$\frac{20+8}{2}$=14���Ƴ�WΪSiԪ�أ��������⣮
��� �⣺����ʯ��è����ǰ20��Ԫ���е�6����ɣ��仯ѧʽΪX3Y2��ZWR4��3T2������Rԭ������������Ϊ�������������3����Rԭ��ֻ����2�����Ӳ㣬����������Ϊ6����RΪOԪ�أ�Y��Z��R��Tλ��ͬ���ڣ������ڵڶ����ڣ�TԪ�������ۣ���TΪFԪ�أ�Z�������������������������ȣ���ZΪBeԪ�أ�YΪ����Ԫ�أ���YΪLi��X��Zλ��ͬ���壬��XΪMgԪ�ػ�CaԪ�أ���XΪþԪ�أ�����X��Rԭ������֮����W��2������$\frac{12+8}{2}$=10���Ƴ�WΪ��Ԫ�ز��������⣬��XΪCaԪ�أ�����X��Rԭ������֮����W��2������$\frac{20+8}{2}$=14���Ƴ�WΪSiԪ�أ��������⣮
A��YΪ�Ԫ�ء�ZΪ��Ԫ�ء�RΪ��Ԫ�ء�TΪ��Ԫ�أ�λ��ͬ���ڣ�Ԫ�ص�ԭ�Ӱ뾶�������Ұ뾶�ڼ�С����ԭ�Ӱ뾶��Y��Z��R��T����A��ȷ��
B��XR2��WR2��������CaO2��SiO2��CaO2��OԪ��Ϊ-1�ۣ�SiO2��OԪ�ػ��ϼ�Ϊ-2����B����
C��WΪ��Ԫ�ء�RΪ��Ԫ�ء�TΪ��Ԫ�أ��ǽ�����F��O��Si������̬�⻯����ȶ���W��R��T����C��ȷ��
D��XΪ��Ԫ�ء�ZΪ��Ԫ�أ�������Ca��Be��������������Ӧ��ˮ������ԣ��������ƣ��������룬��D��ȷ��
��ѡB��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��ƶ�Ԫ���ǽ���Ĺؼ���ע�����պ�������Ų���Ԫ�������ɣ���Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
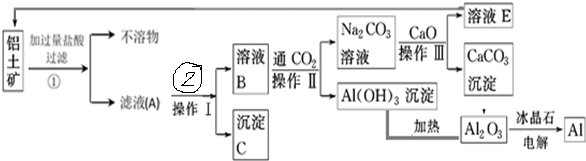
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �����£�17gOH-�����к��е�����ĿΪ8NA | |
| B�� | 78g������C=C˫������ĿΪ3NA | |
| C�� | ��״���£�11.2L��ϩ�к��й��õ��Ӷ���Ŀ3NA | |
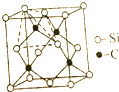
| D�� | �����£�0.1mol SiC���壨������ͼ��������Si-C����ĿΪ0.4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ۢ� | B�� | �ڢܢ� | C�� | �٢ڢ� | D�� | �ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��
��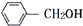 ��Ϊͬϵ�������������Ʒ�Ӧ��
��Ϊͬϵ�������������Ʒ�Ӧ��| A�� | .�ۢܢݢ� | B�� | �٢ڢۢ� | C�� | �٢ڢݢ� | D�� | �٢ڢۢܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | v��A��=0.6 mol/��L•min�� | B�� | v��B��=1.2 mol/��L•min�� | ||
| C�� | v��C��=1.2 mol/��L•min�� | D�� | v��B��=0.03 mol/��L•s�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com