
ijͬѧ����ϡ������п��ȡ������ʵ���У����ּ�����������ͭ��Һ�ɼӿ��������������ʡ���ش��������⣺
��1������ͭ��Һ���Լӿ������������ʵ�ԭ����________________
��2��ʵ����������Na2SO4��CuCl2��MgSO4��K2SO4��4����Һ����������ʵ����CuSO4
��Һ���������õ���________��
��3��Ҫ�ӿ�����ʵ����������������ʣ����ɲ�ȡ�Ĵ�ʩ��________________(������)
��4��Ϊ�˽�һ���о�����ͭ�����������������ʵ�Ӱ�죬��ͬѧ���������һϵ��ʵ�顣�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���ķ�Ӧƿ�У�
�ռ����������壬��¼�����ͬ�������������ʱ�䡣
| ʵ�� �����Һ | A | B | C | D | E | F |
| 4mol/L H2SO 4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| ����CuSO4��Һ /mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O /mL | V7 | V8 | V9 | V10 | 10 | 0 |
��1�� CuSO4��Zn��Ӧ������Cu��Zn�γ�Cu��Zn��أ��ӿ����������������� (2��)
��2�� CuCl2����1�֣�
��3�����߷�Ӧ�¶ȡ��ʵ����������Ũ�ȡ�������п�ıȱ������(2��)��
��4����30��10��17.5����3�֣�
�ڵ�����һ������CuSO4�����ɵĵ���Cu�������Zn�ı��棬������Zn��H2SO4��Һ�ĽӴ������2�֣�
�������������CuSO4��Zn��Ӧ������Cu��Zn�γ�Cu��Zn��أ��ӿ����������������ʣ���������������õ�Ӧ���Ǻ���ͭ���ӵģ�����Ϊ�Ȼ�ͭ��Ӱ�컯ѧ��Ӧ���ʵ������У��¶ȣ�������Ũ�ȣ�ѹǿ����Ӧ��ĽӴ������ABӦ�Ƚϵ�������ͭ��Һ�Ը÷�Ӧ��Ӱ�졣����������Ӧ��A����ͬ������V1=30 �ݱ����֪��CDEFӦ���dz������Ĺ�ϵ����������V6="10" ����ͼ����֪��������ͭ�������ˮ�����֮��ӦΪ20����������V9ӦΪ20��ȥ2.5����17.5. ������������CuSO4��Һʱ���������������ʻ�����ߡ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���Ҫ�����ڵ�����һ������CuSO4�����ɵĵ���Cu�������Zn�ı��棬������Zn��H2SO4��Һ�ĽӴ����
���㣺����Ӱ�컯ѧ��Ӧ�������ص����֪ʶ��


 Сѧ��ĩ���100��ϵ�д�
Сѧ��ĩ���100��ϵ�д� ��ĩ��ϰ���ϵ�д�
��ĩ��ϰ���ϵ�д� ����ѧ�䵥Ԫ������ĩר����100��ϵ�д�
����ѧ�䵥Ԫ������ĩר����100��ϵ�д� �Ƹ�360�ȶ����ܾ�ϵ�д�
�Ƹ�360�ȶ����ܾ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ�������£���ӦN2 + 3H2 2NH3����2L�ܱ������н��У�5min�ڰ�������������1.7 g����Ӧ����Ϊ
2NH3����2L�ܱ������н��У�5min�ڰ�������������1.7 g����Ӧ����Ϊ
| A��v(H2)="0.03" mol/��L��min�� | B��v(N2)="0.02" mol/��L��min�� |
| C��v(NH3)="0.01" mol/��L��min�� | D��v(NH3)="0.17" mol/��L��min�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������·�ӦA2(g)��B2(g) 2AB(g)�ﵽƽ��״̬�ı�־�� ( ��
2AB(g)�ﵽƽ��״̬�ı�־�� ( ��
A��2��(����A2)����(�桢AB)
B�������ڵ���ѹǿ����ʱ����仯
C����λʱ��������n mol AB��ͬʱ������n mol��B2
D��A2��B2��AB�ķ�Ӧ���ʱ�Ϊ2��2��1��״̬
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��7�֣�
��1��Zn����ϡ���ᷴӦһ��ʱ���Ӧ���ʻ�����������Ȼ����Ũ�����Ӧ�������Լӿ졣�ɴ��жϣ�Ӱ�컯ѧ��Ӧ���ʵ������� �� ��
��2��Ϊ̽��п�����ᷴӦ���̵����ʱ仯��ijͬѧ��ʵ��ⶨ�����ǣ���100mlϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���£���������ѻ���Ϊ��״������
| ʱ��/min | 1 | 2 | 3 | 4 | 5 |
| ���/mL | 50 | 120 | 232 | 290 | 310 |
 2NH3(g)(����Ӧ����)���ﵽƽ��ı�־��___ ��
2NH3(g)(����Ӧ����)���ﵽƽ��ı�־��___ ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��5�֣�H2���Դ���ԭNO�Դﵽ������Ⱦ��Ŀ�ģ�
��1����֪����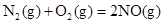
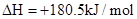
��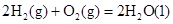
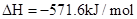
��H2��g����NO��g����Ӧ����N2��g����H2O��l�����Ȼ�ѧ����ʽΪ��________________��
��2��һ�������£������Ϊ2 L��������ͨ��1 mol H2��l mol NO��������N2��g����H2O��l�����÷�Ӧ��ƽ��ʱ�������ڵ�ѹǿ�Ƿ�Ӧ��ʼʱ��40�������������������䣬ֻ����������ͨ��1 mol H2�����㷴Ӧ�ٴ���ƽ��ʱ����ѧƽ�ⳣ��Ϊ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����6�֣�һ���¶��£���һ���ݻ����ܱ������з������¿��淴Ӧ��
2A(g)+B(g) 2C(g) ,�ڷ�Ӧ�����У�C�����ʵ���n(C)��ʱ��ı仯��ϵ����ͼ��ʾ����t1ʱ�俪ʼ�Է�Ӧ��ϵ�����¶ȣ����Իش��������⣺
2C(g) ,�ڷ�Ӧ�����У�C�����ʵ���n(C)��ʱ��ı仯��ϵ����ͼ��ʾ����t1ʱ�俪ʼ�Է�Ӧ��ϵ�����¶ȣ����Իش��������⣺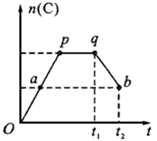
��1��a��ʱ����Ӧ��v������ v���棩���>������<����=������
��2���˷�Ӧ���淴ӦΪ �ȷ�Ӧ����š�����������
��3��a��b���������Ӧ���ʣ�v(a) v(b)
���>������<����=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)�ҹ��зḻ����Ȼ����Դ������Ȼ��Ϊԭ�Ϻϳ����ص���Ҫ��������ͼ��ʾ��ͼ��ijЩת��
���輰������δ�г�����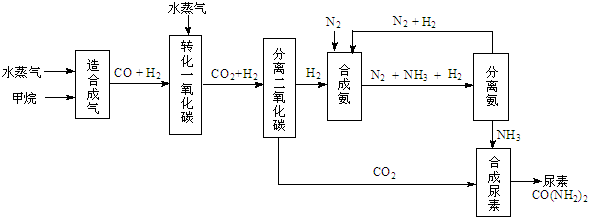
��1������ϳ������������Ȼ�ѧ����ʽ��CH4(g)+H2O(g)  CO(g)+3H2(g)����H��0
CO(g)+3H2(g)����H��0
�ں��º��ݵ������£������CH4�ķ�Ӧ���ʺ�ת���ʣ����д�ʩ���е��� ��
A������ѹǿ B�������¶� C������He�� D������ˮ����Ũ��
| �¶�/�� | 400 | 500 | 800 |
| ƽ�ⳣ��K | 9.94 | 9 | 1 |
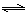 H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£�
H2(g)+CO2(g)���÷�Ӧƽ�ⳣ�����¶ȵı仯���£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��14�֣�����һ����Ҫ�ķǽ���Ԫ�ء���ĵ��ʼ��仯�����ڿ�ѧ�о���ҵ���������Ź㷺����Ҫ�����á�
��1��ij���᳧����β����NO�ķ����ǣ���������ʱ��H2��NO��ԭΪN2��
��֪��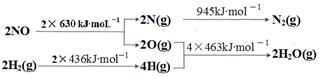
��H2��ԭNO���ɵ�����ˮ�������Ȼ�ѧ����ʽ�ǣ�
��
��2����һ�������£���H2��������̼ת��Ϊ����ķ�Ӧ���£�
CO2(g)+4H2 (g)  CH4 (g)+2H2O(g)
CH4 (g)+2H2O(g)
��һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2 0.2mol��Lһ1��H2 0.8mol��Lһ1��CH40.8mol��Lһ1��H2O1.6mol��Lһ1����CO2��ƽ��ת����Ϊ ��������Ӧ��ƽ�ⳣ������ʽK= ��200��ʱ�÷�Ӧ��ƽ�ⳣ��K=64.8����÷�Ӧ�ġ�H 0���>������<������
��3��ij�о�С����H2��CaCl2�Ʊ�ij�ָƵĻ������֪��Ӧֻ���ɼס������ֻ�����Բ���������֣������������иơ���Ԫ�ص����������ֱ�Ϊ52.29%��46.41%���������ҵ�ˮ��Һ�����ԡ���ش��������⣺
���ҵĻ�ѧʽΪ ��
�ڼ���ˮ��Ӧ�ɵ�H2���仯ѧ����ʽ�ǣ�
��
��4��H2�Ļ��;���ܶ࣬�ɹ������о�С����Ƶ��������л���ˮ�����ȿ��������ˮ�е��л����ʣ�ͬʱ���Ի����������ͼΪһ�ִ������״���ҵ��ˮ��������أ�д���������У����������ĵ缫��Ӧʽ�� ��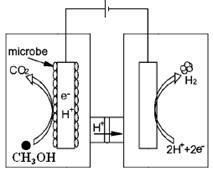
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(14��)��ҵ�����ұ�Ϊԭ����������ϩ�ķ�Ӧ���£�Ph������������
Ph��CH2CH3(g) Ph��CH��CH2(g)+H2(g) ��H
Ph��CH��CH2(g)+H2(g) ��H
ij�о�С��Ϊ̽���¶ȵ����ضԸ÷�Ӧ�IJ���Ӱ�죬���ݻ��ɱ���ܱ������зֱ���������ʵ�飬ʵ��������ͼa��b��ʾ��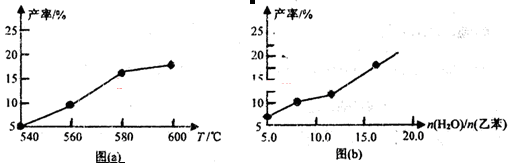
(1)���ݷ�Ӧ����ͼ(a)���жϡ�H 0(�������������������ͬ)����S 0����ѡ�á������˵ķ�Ӧ�¶ȣ� ��
(2)������ʵ����˵���÷�Ӧ�Ѵ�ƽ����� ��
A�����������ܶȲ��ٱ仯
B������������������ֲ���
C������������ϩ����������֮�ȱ��ֲ���
D����λʱ�������ĵ�n(�ұ�)�������ɵ�n(H2)
(3)��ѹǿ���ط�����Ϊ����ұ���ת���ʣ�Ӧ���� ������������ʵ�ʹ�ҵ�����г�����ͨ��ˮ�����ķ�����ˮ�����ĺ����Է�Ӧ��Ӱ��������ͼ(b)��ʾ��
������������ʵ��ʱ��Ӧ�ò��õ�����ʵ�������� ��
A����Ӧ�¶���ͬ B�����ò�ͬ�Ĵ���
C��ѹǿ�������ڳ�ѹ�� D����Ӧ��ͬʱ��ʱ�ⶨʵ������
��ͼ(b)������ ��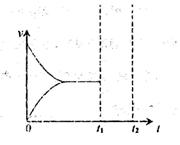
��һ���¶��£��ں�ѹ�ܱ������У�ͨ��һ����n(H2O)/n(�ұ�)��7��1�����壬����������Ӧ����t1ʱ�̴ﵽƽ�⡣���������������䣬��ʱ�����һ������ˮ��������t2ʱ�����´ﵽƽ�⣬������ͼ�л��練Ӧ�ٴδﵽƽ����̵�ͼ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com