

���� ��װ����ԭ��أ�ԭ��طŵ�ʱ���������������ƶ������ݵ�������֪��ͨ�������ĵ缫Ϊ������ͨ�������ĵ缫Ϊ������a���������õ��Ӻ������ӷ�Ӧ����ˮ������������ת�Ƶ���֮��Ĺ�ϵʽ���㣻Pt�缫���������ӣ�˵��Pt�缫Ϊ���������������������������������������ӷŵ���������������C�缫Ϊ������ͭ������C�缫�ŵ�����ͭ�����ǵ�Ƴأ��������ҺŨ�Ȳ��䣬���������������ӷŵ硢�����������ӷŵ磬�缫��Ӧʽ�ֱ�Ϊ��2H++2e-=H2����2Cl--2e-=Cl2�������ݴ�����·��ת�Ƶ�����ȼ����������������
��� �⣺���ݵ�������֪��b�缫�Ǹ�����a�缫���������ŵ�ʱ���������������������a�ƶ��������ϵ缫��ӦʽΪH2-2e-=2H+�����ڱ�״��������O2 11.2L�����ʵ���=$\frac{11.2L}{22.4L/mol}$=0.5mol���ݵ缫��Ӧʽ�����ϵ缫��ӦʽΪO2+4e-+4H+=2H2O��������ת�Ƶ��ӵ����ʵ���0.5mol��4=2mol��Pt�缫���������ӣ�˵��Pt�缫Ϊ���������ӵ�Դ���������������������������������ŵ������������缫��ӦʽΪ4OH--4e-�T2H2O+O2�����ܷ�Ӧ����ʽΪ4AgNO3+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$4Ag+O2��+4HNO3������C�缫Ϊ������ͭ������C�缫�ŵ�����ͭ�����ǵ�Ƴأ��������ҺŨ�Ȳ��䣻����Ag10.8g��Ϊ0.1mol��ת�Ƶ���0.1mol���˹�����Cu�缫ͨ���ĵ�����ĿΪ0.1NA�����������������ӷŵ硢�����������ӷŵ磬�缫��Ӧʽ�ֱ�Ϊ��2H++2e-=H2����2Cl--2e-=Cl2����ת�Ƶ���0.1mol���������������������$\frac{0.1mol}{2}$��2��22.4L/mol=2.24L��
�ʴ�Ϊ��a��H2-2e-=2H+��2������0.1NA��2.24��
���� ���⿼����ԭ��غ͵���ԭ�������ݵ�������ȷ��ԭ������������������Ϸ����ķ�Ӧ���ٽ�ϴ�����·��ת�Ƶ�����Ƚ��м��㣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȫ�� | B�� | �٢ڢ� | C�� | �ڢ� | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ���Ũ�ȵ�NaCl��AlCl3���Һ��ȫ�������õĻ��Һ��pHֵ���� | |
| B�� | NaCl��Һ���һ��ʱ���Ҫ�ָ������ǰ״̬��Ӧ������������ | |
| C�� | Na2SO4��Һ�ڵ������У�������pHֵ���� | |
| D�� | ���CuSO4��Һ��������ӦʽΪ��2H2O+O2+4e-=4OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
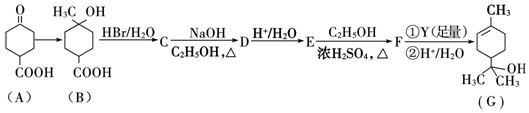
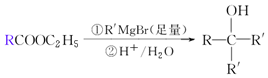
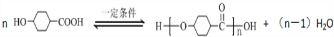 ��
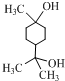
�� ���ٺ˴Ź���������2�����շ� ���ܷ���������Ӧ
���ٺ˴Ź���������2�����շ� ���ܷ���������Ӧ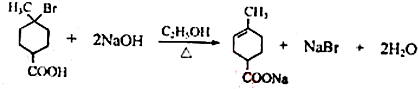 ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��1mol CH3COONa������CH3COOH�γɵ�������Һ�У�CH3COO-��ĿΪNA�� | |
| B�� | 1mol Na��O2��ȫ��Ӧ������Na2O��Na2O2�Ļ���ת�Ƶ�������NA�� | |
| C�� | 7.8gNa2O2�����ˮ��Ӧת�Ƶ�����Ϊ0.1NA | |
| D�� | ��֪N2��g��+3H2��g��?2NH3��g����H=-92.4kJ•mol-1������3NA������ת��ʱ����H��Ϊ-46.2kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 26.3 | B�� | 13.2 | C�� | 19.8 | D�� | ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��NaHSO4��Һ����Ba��OH��2��Һ�����ԣ�H++SO42-+Ba2++OH-�TBaSO4��+H2O | |
| B�� | ����������������Fe��OH��3+3H+�TFe3++3H2O | |
| C�� | ��������ˮ����AuCl4-���Ӻ�NO��Au+4H++4Cl-+NO3-�TAuCl4-+NO��+2H2O | |
| D�� | ��NaClO��Һ���չ�����SO2��ClO-+SO2+H2O�THSO3-+HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2���������������ǻ�ԭ���� | |
| B�� | CuFeS2������ԭ������Ԫ�ر����� | |
| C�� | ÿ����1mol Cu2S����4 mol������ | |
| D�� | ÿת��1.2 mol���ӣ���0.3 mol������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ڢ� | B�� | �٢� | C�� | �٢� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com