
【题目】中国科学院长春应用化学研究所在甲醇燃料电池技术方面获得新突破,组装出了自呼吸电池及主动式电堆.甲醇燃料电池的工作原理如图所示. 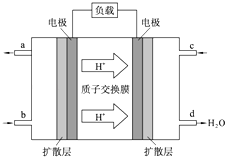
(1)该电池工作时,b口通入的物质为 , c口通入的物质为 .
(2)该电池负极的电极反应式为 .
(3)工作一段时间后,当6.4g甲醇完全反应生成CO2时,有NA个电子转移.
【答案】
(1)CH3OH;O2
(2)CH3OH+H2O﹣6e﹣=CO2+6H+
(3)1.2
【解析】解:(1.)根据装置可以知道d出生成大量的水,所以e口是通入的氧气,故b口通入的是CH3OH,所以答案是:CH3OH;O2;
(2.)乙醇发生氧化反应,在负极放电,总反应式为2CH3OH+3O2=2CO2+4H2O,正极电极反应为:3O2+12e﹣+12H+=6H2O,两式相减可得负极的电极反应式为2CH3OH﹣12e﹣+2H2O=2CO2+12H+ , 即CH3OH﹣6e﹣+H2O=CO2+6H+ . 所以答案是:CH3OH﹣6e﹣+H2O=CO2+6H+;
(3.)甲醇的物质的量为 ![]() =0.2mol,根据反应2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g),当消耗甲醇2mol时,转移电子为12mol,所以当6.4g甲醇完全反应生成CO2时,转移电子是
=0.2mol,根据反应2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g),当消耗甲醇2mol时,转移电子为12mol,所以当6.4g甲醇完全反应生成CO2时,转移电子是 ![]() ×12mol=1.2mol,转移电子数目是1.2NA , 所以答案是:1.2.
×12mol=1.2mol,转移电子数目是1.2NA , 所以答案是:1.2.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.金属镁可用来制造信号弹和焰火
B.某些含铝的化合物可作净水剂
C.硫酸铁可用于治疗缺铁性贫血
D.二氧化硅可用于制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅橡胶是一种医用高分子材料,用于人造心脏、人造乳房、人造肌肉、人造皮肤等,它具有良好的生物相容性和稳定性,有足够的机械强度,而且易于加工、消毒,是一种耐高温橡胶,它是由二甲基二氯硅烷经过两步反应制得的:

(1)其合成反应的反应类型是________反应和________反应。
(2)反应的化学方程式分别为:______________________________________________;
_______________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明某溶液中只含有Fe2+而不含有Fe3+的实验操作是
A. 先滴加氯水,再滴加KSCN溶液后显红色
B. 先滴加KSCN溶液,不显红色,再滴加氯水后显红色
C. 滴加NaOH溶液,产生红褐色沉淀
D. 滴加KSCN溶液,溶液呈红色,再加足量铁粉红色消失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.生命在于运动
B.没有水就没有生命
C.双氧水、医用酒精等外用药可用于皮肤消毒
D.蛋白质遇到( NH4)2SO4、CuSO4等硫酸盐均可发生盐析
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C7H8的某有机物,它能使酸性高锰酸钾溶液褪色,但不能使溴水因化学反应而褪色,在一定条件下与H2完全加成产物的一氯代物的同分异构体有( )
A.3种B.4种C.5种D.6种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。

(1)上图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量变化示意图,请写出N2和H2反应的热化学方程式:____________________________________________________。
(2)已知化学键键能是形成或拆开1 mol化学键放出或吸收的能量,单位kJ/mol。若已知下列(右表)数据,试根据表中及图中数据计算N—H的键能____________kJ/mol。
化学键 | H—H | N≡N |
键能/kJ/mol | 435 | 943 |
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。例如:
4NH3(g)+3O2(g)===2N2(g)+6H2O(g) ; ΔH1=-a kJ/mol ①
N2(g)+O2(g)===2NO(g) ; ΔH2=-b kJ/mol ②
若1 mol NH3还原NO至N2,则反应过程中的反应热ΔH3=________ kJ/mol(用含a、b的式子表示)。
(4)已知下列各组热化学方程式
①Fe2O3(s)+3CO(g) ===2Fe(s)+3CO2(g) ; ΔH1=-25 kJ/mol
②3Fe2O3(s)+CO(g)=== 2Fe3O4(s)+CO2(g) ; ΔH2=-47 kJ/mol
③Fe3O4(s)+CO(g) ===3FeO(s)+CO2(g) ;ΔH3=+640 kJ/mol
请写出FeO(s)被CO(g)还原成Fe和CO2(g)的热化学方程式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯仿(CHCl3)不溶于水,但在一定条件下水解生成两种酸,其中一种是甲酸(HCOOH)。在19世纪氯仿广泛用于麻醉,可由“乙醛漂白粉法”制得。在光照条件下,氯仿易被空气氧化生成剧毒光气(COCl2)和一种化合物。因此氯仿需要小口钢罐贮存运输,使用前要检验其是否变质。
(1)CHCl3的电子式为____,COCl2的分子构型为____,HCOOH中C的杂化方式为____;
(2)漂白粉中三种元素的简单离子的半径的大小顺序为____(用离子符号表示);
(3)为了检验氯仿是否变质,可向其中加入____,观察到 的现象,即可确认其已变质;
(4)Fe2+的外围电子排布图为____;
(5)纯铁的一种同素异形体的晶胞为面心立方晶胞,该晶体中原子的配位数为____,若铁原子的半径为a cm,则该晶体的密度为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com