
��10�֣����û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ���壮
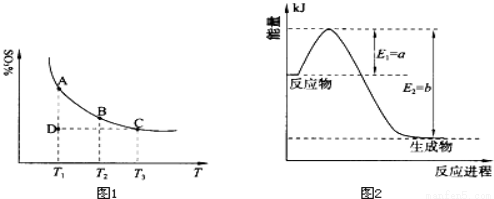
��1�����������У�SO2����������SO3��2SO2��g��+O2��g�� 2SO3��g���������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
2SO3��g���������ϵ��SO3�İٷֺ������¶ȵĹ�ϵ����ͼ1��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣺
�ٺ��¡���ѹ�����£���Ӧ2SO2��g��+O2��g�� 2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����ƽ�� �ƶ�������������ҡ���������
2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����ƽ�� �ƶ�������������ҡ���������
�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1 K2�����������������=������ͬ��������Ӧ���е�״̬Dʱ��v�� v�棨���������������=������
��2�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũҵ������������������Ҫ���ã�
����ͼ2��һ�����¶Ⱥ�ѹǿ����N2��H2��Ӧ����1molNH3�����������仯ʾ��ͼ����д����ҵ�ϳɰ����Ȼ�ѧ��Ӧ����ʽ�� ������H����ֵ�ú���ĸa��b�Ĵ���ʽ��ʾ��
�ڰ�������ˮ�õ���ˮ����25���£���a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һǡ�������ԣ��ú�a��b�Ĵ���ʽ��ʾ����ˮ�ĵ���ƽ�ⳣ������ʽ ��
��3����֪25��CʱKsp[AgCl]=1.6��10-10mol2?L-2��Ksp[AgI]=1.5��10-16mol2?L-2������25���£���0.1L0.002mol?L-1��NaCl��Һ����μ���0.1L0.002mol?L-1��������Һ���а�ɫ�������ɣ��ӳ����ܽ�ƽ��ĽǶȽ��Ͳ���������ԭ���� ����Ӧ�����Һ�У���������0.1L0.002mol?L-1��NaI��Һ�������������� �������������ԭ���ǣ������ӷ���ʽ��ʾ�� ��
��1���� ���� �� �� �� ��
��2����N2��g��+3H2��g�� 2NH3��g����H=-2��b-a��kJ?mol-1 ���� 10-7b/(a-b)��
2NH3��g����H=-2��b-a��kJ?mol-1 ���� 10-7b/(a-b)��
��3��c(Ag+)(Cl-)�����ܶȻ�Ksp��AgCl���� ��ɫ����ת��Ϊ��ɫ���� AgCl��s��+I-�TAgI��s��+Cl-��
��������
����������ٺ��¡���ѹ�����£���Ӧ2SO2��g��+O2��g�� 2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����Ϊ�˱���ѹǿ���䣬���������ݻ���Ҫ����ʹ��Ӧ��ϵ�ĸ������ʵ�Ũ�ȶ���С�����ڷ�Ӧ��ϵ����С�ı����࣬����ƽ�������ƶ�������ͼ���֪�������¶ȣ�SO3��ƽ�⺬����С��˵�������¶�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴Ӧ���������ȷ�Ӧ����˸÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ԡ�H<0����Ϊ�����¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С�����������¶�ΪT1<T2����Ӧ�ﵽƽ��״̬״̬ʱ��ƽ�ⳣ���ֱ�ΪK1>K2������Ӧ���е�״̬Dʱ����Ӧδ�ﵽ���¶��µ�ƽ��״̬��SO3�ĺ�������ƽ��״̬�����Է�Ӧ������У����v��>v��; (2)�ٸ���ͼʾ��֪�ڹ�ҵ�ϳɰ����Ȼ�ѧ��Ӧ����ʽ��N2��g��+3H2��g��
2SO3��g����ƽ�⣬����ϵ��ͨ�뺤����Ϊ�˱���ѹǿ���䣬���������ݻ���Ҫ����ʹ��Ӧ��ϵ�ĸ������ʵ�Ũ�ȶ���С�����ڷ�Ӧ��ϵ����С�ı����࣬����ƽ�������ƶ�������ͼ���֪�������¶ȣ�SO3��ƽ�⺬����С��˵�������¶�ƽ�������ƶ�������ƽ���ƶ�ԭ���������¶ȣ�ƽ�������ȷ�Ӧ�����ƶ����淴Ӧ���������ȷ�Ӧ����˸÷�Ӧ������Ӧ�Ƿ��ȷ�Ӧ�����ԡ�H<0����Ϊ�����¶ȣ�ƽ�������ƶ���ƽ�ⳣ����С�����������¶�ΪT1<T2����Ӧ�ﵽƽ��״̬״̬ʱ��ƽ�ⳣ���ֱ�ΪK1>K2������Ӧ���е�״̬Dʱ����Ӧδ�ﵽ���¶��µ�ƽ��״̬��SO3�ĺ�������ƽ��״̬�����Է�Ӧ������У����v��>v��; (2)�ٸ���ͼʾ��֪�ڹ�ҵ�ϳɰ����Ȼ�ѧ��Ӧ����ʽ��N2��g��+3H2��g�� 2NH3��g����H=-2��b-a��kJ/mol������25���£���a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һǡ�������ԣ���c(NH4+)=c(Cl-);�������ǰ�ˮ���Ȼ�淋Ļ����Һ��NH3.H2O
2NH3��g����H=-2��b-a��kJ/mol������25���£���a mol?L-1�İ�ˮ��b mol?L-1������������ϣ���Ӧ����Һǡ�������ԣ���c(NH4+)=c(Cl-);�������ǰ�ˮ���Ȼ�淋Ļ����Һ��NH3.H2O NH4++OH-��c(NH4+)=b/2mol/L; c(OH-)=10-7mol/L������NԪ���غ�ɵ�c(NH3.H2O)=(a��b)/2mol/L,���ð�ˮ�ĵ���ƽ�ⳣ������ʽK=
NH4++OH-��c(NH4+)=b/2mol/L; c(OH-)=10-7mol/L������NԪ���غ�ɵ�c(NH3.H2O)=(a��b)/2mol/L,���ð�ˮ�ĵ���ƽ�ⳣ������ʽK=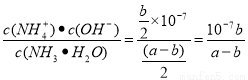 ����3����֪25��CʱKsp[AgCl]=1.6��10-10mol2?L-2��Ksp[AgI]=1.5��10-16mol2?L-2������25���£���0.1L0.002mol?L-1��NaCl��Һ����μ���0.1L0.002mol?L-1��������Һ������c(Ag+)��c(Cl-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.6��10-10mol2?L-2 =Ksp[AgCl]�������а�ɫ�������ɣ��ڸ�����Һ�д���AgCl�ij����ܽ�ƽ�⣬����Ӧ�����Һ�У���������0.1L0.002mol?L-1��NaI��Һ������c(Ag+) ��c(I-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.5��10-16 mol2?L-2 =Ksp[AgI]�����Ի����������ת������ɫ����ת��Ϊ��ɫ���������ӷ���ʽ��AgCl��s��+I-�TAgI��s��+Cl-��
����3����֪25��CʱKsp[AgCl]=1.6��10-10mol2?L-2��Ksp[AgI]=1.5��10-16mol2?L-2������25���£���0.1L0.002mol?L-1��NaCl��Һ����μ���0.1L0.002mol?L-1��������Һ������c(Ag+)��c(Cl-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.6��10-10mol2?L-2 =Ksp[AgCl]�������а�ɫ�������ɣ��ڸ�����Һ�д���AgCl�ij����ܽ�ƽ�⣬����Ӧ�����Һ�У���������0.1L0.002mol?L-1��NaI��Һ������c(Ag+) ��c(I-)=0.001mol/L��0.001mol/L=1��10-6mol2/L2>> 1.5��10-16 mol2?L-2 =Ksp[AgI]�����Ի����������ת������ɫ����ת��Ϊ��ɫ���������ӷ���ʽ��AgCl��s��+I-�TAgI��s��+Cl-��
���㣺������������Ի�ѧƽ���ƶ���Ӱ�졢�ε�ˮ�⡢������ʵ���ƽ�ⳣ���ı�������ܽ�ƽ�������Ӧ�ü�������ת����֪ʶ��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014��2015��ӱ�ʡ��һ��һѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���з�Ӧ����������ԭ��Ӧ���� (����)
A��CaCO3��2HCl===CaCl2��CO2����H2O B��CO2��H2O===H2CO3
C��2H2O2���� 2H2O��O2�� D��CaCO3 CaO��CO2��
CaO��CO2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
25 ��ʱ����0.01 mol��L��1��������Һ�У�ˮ�������H��Ũ����
A��5��10��13 mol��L��1 B��0.02 mol��L��1
C��1��10��7 mol��L��1 D��1��10��12 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�B�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��CH3CH2CH2CH3(g)��6��5O2(g) == 4CO2(g)��5H2O(l) ��H����2 878 kJ��mol-1
(CH3)2CHCH3(g)��6��5O2(g) == 4CO2(g)��5H2O(l) ��H����2 869kJ��mol-1 ����˵����ȷ����
A�� ��������Ӵ�������������춡����� B�� ��������ȶ��Դ����춡��
C�� �춡��ת��Ϊ������Ĺ�����һ�����ȹ��� D�� �춡������е�̼�����������Ķ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�B�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�ס������������ڶ��ڽ���A��B�ķ�Ӧ������ÿ���Ӽ���4mol A������ÿ���Ӽ���2mol A�����������еķ�Ӧ����
A���� B���ҿ� C����� D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�A�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�ö��Ե缫�������ͭ��Һ����������ת�Ƶ��ӵ����ʵ������������������Ĺ�ϵ��ͼ��ʾ(�������������ͬ״���²ⶨ)����ʹ��Һ�ָ�����ʼ״̬��������Һ�м���(����)

A��0.15 mol CuO�� B��0.1 mol CuCO3
C��0.075mol Cu(OH)2 D��0.05 mol Cu2(OH)2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У���߶�9���¿�A�㻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����Һ�������25�棬�����й�������ȷ����( )
A��PHֵ��ͬ��������Ȼ����Һ��ˮ�ĵ���̶���ͬ
B��ij��Һ����ˮ�������c(H+)=10-13,�����Һ��PHһ��Ϊ13
C��pH=4.5�ķ���֭��c(H+)��pH=6.5��ţ����c(H+)��2��
D���к�Ũ�Ⱥ��������ͬ������ʹ��ᣬ���ĵ��������Ƶ����ʵ���֮��Ϊ1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��2015ѧ�꽭�����ݸ�����ѧ��У����һ9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ʵ��������Ҫ����2mol/L��NaCl��Һ950mL������ʱӦѡ�õ�����ƿ�Ĺ��ͳ�ȡNaCl�����ֱ��� �� ��
A��950mL��111.2g B��500mL��117g C��1000mL��117g D��1000mL��111.2g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�����и߶���ѧ�����л�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
ij�����ķ����л���������п�ۺ�����ͭ(�����ɷֲ����ᷴӦ)��������������Ӵ��γ���ˮ������������������ˮ�����������ҷ�Ӧ��������ʣ�࣬��ʱ��ˮ��һ�����еĽ���������
A��Fe2+��Cu2+ B��Cu2+ ��H+
C��Zn2+ ��Fe2+ D��Zn2+ ��H+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com