
[化学——选修5:有机化学基础](15分)
某有机物A的水溶液显酸性,遇FeCl3溶液不显色,A分子结构中不含甲基,含苯环,苯环上的一氯代物只有两种, A和其他有机物存在如下图所示的转化关系:
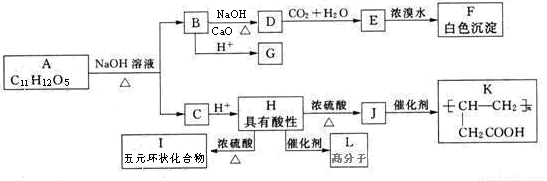
已知: 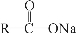 + NaOH
+ NaOH 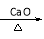 R—H + Na2CO3
R—H + Na2CO3
试回答下列问题:
(1)B化学式 ,G的化学名称是 。
(2)H→I反应类型为 ,J所含官能团的名称为 。
(3)写出H→L 反应的化学方程式 。
(4)A的结构简式 。
(5)F的同分异构体中含有苯环且官能团相同的物质共有 种(不包括F),其中核磁共振氢谱有两个峰,且峰面积比为1︰2的是 (写结构简式)。
(1)C7H4O3Na2 (2分),对羟基苯甲酸(2分)
(2)酯化(1分),碳碳双键和羧基(各1分)
(3)n HO-CH2-CH2-CH2COOH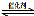
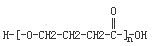 +(n-1)H2O;(2分)
+(n-1)H2O;(2分)
(4) 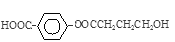 (2分)
(2分)
(5)5种 ,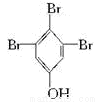 。 (各2分)
。 (各2分)
【解析】
试题分析:(1)由题意可知,A中不含有酚羟基,苯环上的一氯代物只有两种,说明A的苯环上有2个不同的对位取代基;E与浓溴水反应生成白色沉淀,所以E是苯酚,D是苯酚钠,B到D发生脱羧反应,下去1个羧基,所以B是对羟基苯甲酸与氢氧化钠反应的产物,化学式为C7H4O3Na2;G是B酸化后的产物,所以G是对羟基苯甲酸;
(2)因为A中不含有酚羟基,所以G中的酚羟基来自于A的水解反应,说明A中的酯基的碳氧单键与苯环直接相连;由K的结构简式可倒推A中含有HO(CH2)3COO-结构,所以另一取代基为-COOH;A为酯类化合物,与氢氧化钠反应后生成B、C;C为HO(CH2)3COONa,H为HO(CH2)3COOH,所以H到I是分之内的酯化反应;H在浓硫酸、加入条件下发生消去反应生成J,所以J为CH2=CHCH2COOH,含有碳碳双键、羧基;
(3)H到L发生缩聚反应,化学方程式为n HO-CH2-CH2-CH2COOH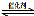
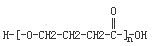 +(n-1)H2O;
+(n-1)H2O;
(4)由以上分析A的结构简式为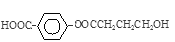 ;
;
(5)F是三溴苯酚,含有苯环且官能团相同的同分异构体的判断方法是,先写出三溴苯的同分异构体共有3种,然后再把羟基作取代基,计算三溴苯的一代物的种数,也即计算三溴苯的等效氢种数,除去F外还有5种。其中核磁共振氢谱有两个峰,且峰面积比为1︰2的是 。
。
考点:考查有机物的化学性质及推断,同分异构体的判断,化学式、化学方程式的判断及书写


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
化学与科学、技术、社会和环境密切相关。下列说法正确的是( )
A.化学平衡常数是指一定条件下的可逆反应,生成物浓度的幂之积与反应物浓度的幂之积的比值。
B.已知4HCl(g)+O2(g)=2H2O(g)+2Cl2(g) 能自发进行,则该反应ΔH<0,ΔS>0
C.其他条件不变,增大压强,平衡可能移动,但平衡常数一定不变
D.铁制品表面镶锌块和铁制品表面镀锡,都能起到防腐的作用且防腐原理是相同的
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列与金属腐蚀有关的说法正确的是( )
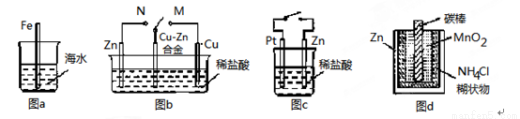
A.图a中,插入海水中的铁棒越靠近底端腐蚀越严重
B.图b中,开关由M改置于N时,Cu-Zn合金的腐蚀速率减小
C.图c中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大
D.图d中,Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三终极预测理综化学试卷(解析版) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。
(1)卤族元素位于元素周期表的_________区;溴的价电子排布式为____________________。
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的。使氢氟酸分子缔合的作用力是________。
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是_________。
| 氟 | 氯 | 溴 | 碘 |
第一电离能 (kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图I、II所示:
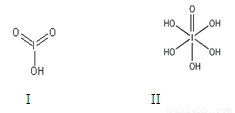
请比较二者酸性强弱:HIO3_____ H5IO6(填“>”、 “<”或“=”)。
(5)已知ClO2- 为角型,中心氯原子周围有四对价层电子。ClO2- 中心氯原子的杂化轨道类型为___________,写出一个ClO2- 的等电子体__________。
(6)下图为碘晶体晶胞结构。有关说法中正确的是_____________。
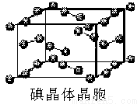
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
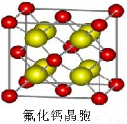
(7)已知CaF2晶体(见图)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为___________。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三终极预测理综化学试卷(解析版) 题型:选择题
分子式为C5H12O的醇与和它相对分子质量相同的一元羧酸进行酯化反应,生成的酯共有(不考虑立体异构)
A.15种 B.16种 C.17种 D.18种
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三第三次模拟考试理综化学试卷(解析版) 题型:实验题
酸性KMnO4溶液能与草酸(H2C2O4)溶液反应。某探究小组利用反应过程中溶液紫色消失快慢的方法来研究影响反应速率的因素。
Ⅰ.实验前首先用浓度为0.1000mol?L-1酸性KMnO4标准溶液滴定未知浓度的草酸。
(1)写出滴定过程中发生反应的化学方程式为 。
(2)滴定过程中操作滴定管的图示正确的是 。
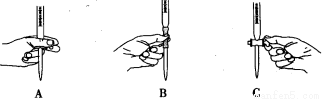
(3)若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的草酸溶液浓度
(填“偏高”、“偏低”、或“不变”)。
Ⅱ.通过滴定实验得到草酸溶液的浓度为0.2000mol·L-1 。用该草酸溶液按下表进行后续实验(每次实验草酸溶液的用量均为8mL)。
实验编号 | 温度(℃) | 催化剂 用量(g) | 酸性高锰酸钾溶液 | 实验目的 a. 实验1和2探究 ;
b. 实验1和3探究反应物浓度对该反应速率的影响;
c. 实验1和4探究催化剂对该反应速率的影响。 | |
体积 (mL) | 浓度 (mol?L-1) | ||||
1 | 25 | 0.5 | 4 | 0.1000 | |
2 | 50 | 0.5 | 4 | 0.1000 | |
3 | 25 | 0.5 | 4 | 0.0100 | |
4 | 25 | 0 | 4 | 0.1000 | |
(4)写出表中a 对应的实验目的 ;若50°C时,草酸浓度c(H2C2O4)随反应时间t的变化曲线 如下图所示,保持其他条件不变,请在图中画出25°C时c(H2C2O4)随t的变化曲线示意图。

(5)该小组同学对实验1和3分别进行了三次实验,测得以下实验数据(从混合振荡均匀开始计时):
实验编号 | 溶液褪色所需时间(min) | ||
第1次 | 第2次 | 第3次 | |
1 | 14.0 | 13.0 | 11.0 |
3 | 6.5 | 6.7 | 6.8 |
分析上述数据后得出“当其它条件相同时,酸性高锰酸钾溶液的浓度越小,褪色时间就越短,即反应速率就越快”的结论。甲同学认为该小组“探究反应物浓度对速率影响”的实验方案设计中存在问题,从而得到了错误的实验结论,请简述甲同学改进的实验方案 。
(6)该实验中使用的催化剂应选择MnSO4而不是MnCl2,原因可用离子方程式表示为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高三第三次模拟考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.装饰材料中的甲醛和芳香烃会造成居室污染
B.石蜡油分解产生的气体不能使酸性高锰酸钾溶液褪色
C.分子组成为CH2Cl2和C2H6O的有机物都存在同分异构现象
D.油脂、葡萄糖、蛋白质都是人体重要的营养物质,它们都能发生水解反应
查看答案和解析>>
科目:高中化学 来源:2013-2014黑龙江省高二下学期期末考试化学试卷(解析版) 题型:选择题
下列实验中,颜色的变化与氧化还原反应无关的是
A.SO2使酸性KMnO4溶液褪色
B.Na2O2投入酚酞溶液中溶液先变红后褪色
C.向FeSO4溶液中滴NaOH溶液,生成的沉淀由白色变成灰绿色,最后变成红褐色
D.往紫色石蕊试液中通入氨气,溶液变蓝
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com