
【题目】由下列实验及现象不能推出相应结论的是( )
实验 | 现象 | 结论 | |
| 向2mL0.1mol/L FeCl3 溶液中加足量铁粉,震荡,加 | 黄色逐渐消失,加 | 还原性: |
| 将金属钠在燃烧匙中点燃,迅速伸入集满 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 |
|
| 加热盛有少量 | 石蕊试纸变蓝 |
|
| 向 | 一支试管中产生黄色沉淀,另一支中无明显现象 |
|
A. A B. B C. C D. D
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+ 4B(g)![]() C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
C(g)+ D(g),在四种不同情况下的反应速率如下,其中反应进行得最快的是( )
A. vA=0.15mol/(L·min) B. vB=0.6 mol/(L·min)
C. vC=0.4 mol/(L·min) D. vD=0.01 mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢气体生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。
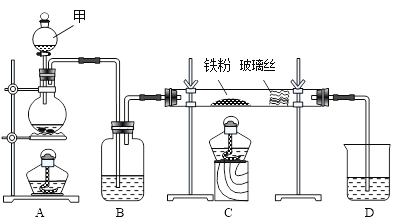
回答下列问题:
(1)制取无水氯化铁实验中,仪器甲的名称为_______________,进行实验时,应先点燃___________(选填A或C)处酒精灯。
(2)制取无水氯化铁的实验中,A中反应的离子方程式为_______________________,装置B中加入的试剂是____________________。
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是__________________(化学方程式表示)。为除去氯气中混有的少量HCl,可以在装置A、B间加入装有_______________的洗气瓶。
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____________(填化学式)。长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____________(填数字代号)。
① O2 ② Cl2 ③ CO2 ④ HClO
(5)制取无水氯化亚铁实验中,装置A用来制取HCl气体,其化学方程式为:NaCl +H2SO4 (浓) ![]() NaHSO4+ HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主要问题是_________________________________________。
NaHSO4+ HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主要问题是_________________________________________。
(6)制取无水氯化亚铁实验中,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是________________。(填化学式)欲制得纯净的FeCl2,在实验操作中应先__________________________,再___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示是![]() 的两个性质实验,下列有关说法中正确的是
的两个性质实验,下列有关说法中正确的是![]()
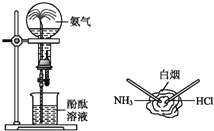
A. 两个实验均表现了![]() 易溶于水
易溶于水
B. 两个实验均表现了![]() 易挥发
易挥发
C. 两个实验均表现了![]() 是碱性气体
是碱性气体
D. 两个实验均表现了![]() 是还原性气体
是还原性气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】人体内磷脂的重要生理作用是( )
A. 细胞膜结构的重要成分 B. 氧化分解为机体提供能量
C. 合成维生素D和脂肪的原料 D. 有利于脂溶性物质的吸收
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲酸香叶酯是一种食品香料.可以由香叶醇与甲酸发生酯化反应制得.下列说法中正确的是( ) 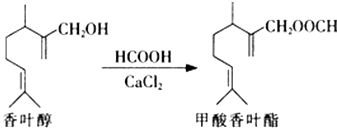
A.香叶醇的分子式为C11H18O
B.香叶醇在浓硫酸、加热条件下可发生消去反应
C.1 mol甲酸香叶酯可以与2 molH2发生加成反应
D.甲酸香叶酯分子中所有碳原子均可能共平面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的“氧化物”样品,用5mol/L盐酸0.14L恰好完全反应,所得溶液还能吸收标准状况下2.24L氯气,使其中Fe2+全部转化为Fe3+.该样品可能的化学式是( )
A. Fe5O6 B. Fe3O4 C. Fe6O7 D. Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水泥是重要的建筑材料.水泥熟料的主要成分为![]() 、
、![]() ,并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
,并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
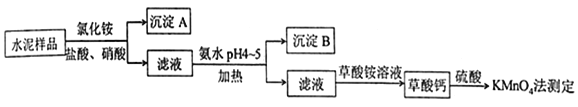
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸.加入硝酸的目的是________,还可使用________代替硝酸.
(2)沉淀![]() 的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________________________________________
的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________________________________________
(3)加氨水过程中加热的目的是__________________.沉淀![]() 的主要成分为________、________(填化学式).
的主要成分为________、________(填化学式).
(4)草酸钙沉淀经稀![]() 处理后,用
处理后,用![]() 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为: ![]() .实验中称取
.实验中称取![]() 水泥样品,滴定时消耗了
水泥样品,滴定时消耗了![]() 的
的![]() 溶液
溶液![]() ,则该水泥样品中钙的质量分数为________.
,则该水泥样品中钙的质量分数为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com