
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素,D的最外层电子数是其内层电子数的三倍。已知:①热稳定性:HmD>HmC;②![]() 、
、![]() 具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
(1)![]() 的电子式:_____________。
的电子式:_____________。
(2)![]() 、
、![]() 的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
(3)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的离子方程式______________________________。
(4)A和E形成的化合物,其晶体类型属___________;该晶体中离A最近的A有_____个。A和E形成化合物的熔点比C和E形成化合物的熔点_________(填高或低)。
(5)常温下,将等物质的量浓度的![]() 溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
查看答案和解析>>
科目:高中化学 来源:重庆市南开中学2010届高三下学期5月月考(理综化学部分) 题型:填空题
(15分)A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素,D的最外层电子数是其内层电子数的三倍。已知:①热稳定性:HmD>HmC;②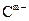 、
、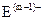 具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
(1)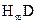 的电子式:_____________。
的电子式:_____________。
(2)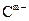 、
、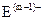 的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
(3)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的离子方程式______________________________。
(4)A和E形成的化合物,其晶体类型属___________;该晶体中离A最近的A有_____个。A和E形成化合物的熔点比C和E形成化合物的熔点_________(填高或低)。
(5)常温下,将等物质的量浓度的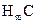 溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
查看答案和解析>>
科目:高中化学 来源:重庆市2010届高三下学期5月月考(理综化学部分) 题型:填空题
(15分)A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素,D的最外层电子数是其内层电子数的三倍。已知:①热稳定性:HmD>HmC;② 、
、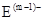 具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
(1)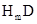 的电子式:_____________。
的电子式:_____________。
(2) 、
、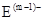 的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
(3)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的离子方程式______________________________。
(4)A和E形成的化合物,其晶体类型属___________;该晶体中离A最近的A有_____个。A和E形成化合物的熔点比C和E形成化合物的熔点_________(填高或低)。
(5)常温下,将等物质的量浓度的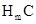 溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是位于短周期的主族元素,其中A、B为金属元素,D的最外层电子数是其内层电子数的三倍。已知:①热稳定性:HmD>HmC;②![]() 、
、![]() 具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
具有相同的电子层结构;③B与E在同一周期,在该周期中,E的原子半径最小,B的离子半径最小;④A、B所形成的单核离子具有相同的电子层结构,B的最高价氧化物对应的水化物与A、E的最高价氧化物对应的水化物都能反应。依据上述信息回答下列问题:
(1)![]() 的电子式:_____________。
的电子式:_____________。
(2)![]() 、
、![]() 的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
的还原性强弱为_________>___________,能证明其还原性强弱的离子方程式为____________________________。
(3)写出B的最高价氧化物对应的水化物和A的最高价氧化物对应的水化物反应的离子方程式______________________________。
(4)A和E形成的化合物,其晶体类型属___________;该晶体中离A最近的A有_____个。A和E形成化合物的熔点比C和E形成化合物的熔点_________(填高或低)。
(5)常温下,将等物质的量浓度的![]() 溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
溶液和A的最高价氧化物对应的水化物溶液等体积混合,所得溶液显碱性,溶液中离子浓度由大到小的顺序为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com