
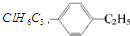
 表示的有机物中,能发生消去反应的卤代烃共有( )
表示的有机物中,能发生消去反应的卤代烃共有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 根据苯环左边的取代基共有5种:CH2ClCH2CH2-、CH3CHClCH2-、CH3CH2CHCl-、CH3(CH2Cl)CH-、(CH3)2CCl-,该5种结构都能够发生消去反应.
解答 解:苯环左边的取代基-C3H6Cl的同分异构体数目决定了该有机物能够发生消去反应的卤代烃数目,
-C3H6Cl的同分异构体有:CH2ClCH2CH2-、CH3CHClCH2-、CH3CH2CHCl-、CH3(CH2Cl)CH-、(CH3)2CCl-,总共有5种,
则结构简式 表示的有机物中能发生消去反应的卤代烃共有5种,
表示的有机物中能发生消去反应的卤代烃共有5种,
故选D.
点评 本题考查了同分异构体书写及判断,题目难度不大,明确同分异构体的书写原子为解答关键,试题侧重考查学生的分析能力及灵活运用能力.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3═2Na++CO32- | B. | Al2(SO4)3═2 Al3 ++3SO42- | ||
| C. | H2CO3?2H++HCO3- | D. | NH3•H2O?NH4++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )
在电解质溶液的导电性装置(如图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是( )| A. | 盐酸中逐滴加入食盐溶液 | B. | 硫酸中逐滴加入氢氧化钠溶液 | ||
| C. | 硫酸中逐滴加入氢氧化钡溶液 | D. | 醋酸中逐滴加入氨水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | N2(g)与O2(g)反应生成NO(g)是放热反应 | |
| B. | 2 mol O原子结合生成O2(g)时需要吸收498 kJ能量 | |
| C. | 1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量 | |
| D. | N2(g)+O2(g)=2NO(g)的反应热△H=+1444 kJ•molˉ1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属甲的阳离子比同价态的金属乙的阳离子氧化性强,则金属甲比金属乙活泼 | |
| B. | 原电池中电子从负极经过溶液流向正极 | |
| C. | 电解池中电解质溶液的阳离子向阴极迁移 | |
| D. | 在铁制品上镀银,铁做正极,银做负极 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 铜平均溶解速率(10-3mol•L-1•min-1) | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com