常温常压下,将amolCO2气体通入1L1mol/L的NaOH溶液中,下列对所得溶液的描述不正确的是( )
A.当a=0.5时,所得溶液中存在:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
B.当0.5<a<1时,所得溶液中存在:c(Na+)>c(CO32-)+c (HCO3-)+c (H2CO3)
C.当a=1时,所得溶液中存在:c(CO32-)+c(OH-)=c (H+)+c (H2CO3)
D.当a=1时,所得溶液中存在:c(Na+)>c (CO32-)>c(HCO3-)>c(OH-)>c(H+)
【答案】
分析:NaOH溶液中n(NaOH)=1L×1mol/L=1mol,当a:1
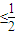
,二氧化碳和氢氧化钠反应生成碳酸钠,当a:1≥1时二氧化碳和氢氧化钠反应生成碳酸氢钠,当
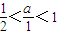
时,二氧化碳和氢氧化钠反应生成碳酸氢钠和碳酸钠,根据溶液中的溶质分析解答.
解答:解:A.当a=0.5时,二氧化碳和氢氧化钠反应生成0.5mol碳酸钠,钠离子不水解,碳酸根离子水解,所以c(Na
+)>c(CO
32-),碳酸根离子和碳酸氢根离子水解都产生氢氧根离子,但水解较微弱,且只有碳酸根离子水解产生碳酸氢根离子,所以c(CO
32-)>c(OH
-)>c(HCO
3-),故A正确;
B.当0.5<a<1时,二氧化碳和氢氧化钠反应生成碳酸氢钠和碳酸钠,根据物料守恒知,碳酸氢钠中存在c(Na
+)=c(CO
32-)+c (HCO
3-)+c (H
2CO
3),碳酸钠中存在c(Na
+)=2c(CO
32-)+2c (HCO
3-)+2c (H
2CO
3),所以混合溶液中存在c(Na
+)>c(CO
32-)+c (HCO
3-)+c (H
2CO
3),故B正确;
C.当a=1,二氧化碳和氢氧化钠恰好反应生成碳酸氢钠,根据物料守恒知,碳酸氢钠中存在c(Na
+)=c(CO
32-)+c (HCO
3-)+c (H
2CO
3)①,根据电荷守恒知,c(Na
+)+c (H
+)=2c(CO
32-)+c (HCO
3-)+c (OH
-)②,将②-①得c(CO
32-)+c(OH
-)=c (H
+)+c (H
2CO
3),故C正确;
D.当a=1,二氧化碳和氢氧化钠恰好反应生成碳酸氢钠,溶液中HCO
3-水解程度大于HCO
3-电离程度,且水解和电离程度都较小,主要以HCO
3-形式存在,则c(HCO
3-)>c(CO
32-),故D错误;
故选D.
点评:本题考查离子浓度的大小比较,题目难度中等,明确二氧化碳和氢氧化钠反应的量是解本题关键,注意把握弱电解质的电离和盐类水解的原理,从守恒的角度比较离子浓度大小是常用的方法.

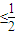 ,二氧化碳和氢氧化钠反应生成碳酸钠,当a:1≥1时二氧化碳和氢氧化钠反应生成碳酸氢钠,当
,二氧化碳和氢氧化钠反应生成碳酸钠,当a:1≥1时二氧化碳和氢氧化钠反应生成碳酸氢钠,当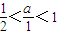 时,二氧化碳和氢氧化钠反应生成碳酸氢钠和碳酸钠,根据溶液中的溶质分析解答.
时,二氧化碳和氢氧化钠反应生成碳酸氢钠和碳酸钠,根据溶液中的溶质分析解答.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案